2. 常州大学 材料科学与工程学院,常州 213164
2. School of Materials Science and Engineering, Changzhou University, Changzhou 213164, China
钛及钛合金由于其良好的力学性能、抗腐蚀性能和优良的生物相容性[1-2],被广泛用做骨科植入体[3-5]。钛种植体的主要问题是生物活性差和不具有抗菌性能,二者是目前植入体失败的两大重要原因。因此,提高种植体的生物活性和抗菌性能是提高种植体长期稳定的关键。TiO2具有良好的化学稳定性、生物相容性以及和钛合金基体结合强等优点,被广泛用于钛合金种植体的表面改性[6],但TiO2涂层的生物活性有待进一步提高。在前期工作中,作者基于等离子体喷涂技术特殊的热历史条件,通过在TiO2涂层中掺入Nb2O5制备了具有微纳米结构的Nb2O5-TiO2复合涂层,实现了对涂层表面微纳米结构的调控。细胞实验结果表明,与TiO2涂层相比,Nb2O5-TiO2复合涂层具有更佳的生物活性[7]。但该涂层仍不具有抗菌性能,限制其在种植体表面改性方面的潜在应用。
目前的研究表明通过在表面涂层中添加抗菌元素(银、镓等)[8-9],抗菌多肽[10-12]或抗生素[13-15]等可赋予种植体抗菌性能。因可操作性高、成本低以及抗菌效果显著等优点,抗菌元素掺杂在植入体表面改性方面得到了广泛使用。铜离子是人体所必需的微量元素,参与大部分组织器官的新陈代谢过程[16]。它能够促进血管化[17],提高骨愈合速率[18]。相关研究表明,与锌离子和银离子相比,铜离子具有良好的抗菌性能和较好的细胞兼容性[19]。Zhang Lan等[20]用阳极氧化的方法在钛合金表面制备了铜掺杂涂层,并验证了涂层的抗菌性能和生物相容性。研究结果表明铜离子掺杂显著提高了涂层对大肠杆菌和金黄色葡萄球菌的抑制,同时能够促进小鼠成纤维细胞的增殖。因此,鉴于铜离子的优点,为赋予Nb2O5-TiO2涂层抗菌性能,将一定比例的CuO掺杂在Nb2O5-TiO2涂层中,考察掺杂CuO后对Nb2O5-TiO2涂层物化性能的影响,利用金黄色葡萄球菌和大肠杆菌评价涂层的抗菌性能,利用小鼠颅顶前骨细胞亚克隆14(MC3T3-E1 Subclone 14)评价涂层的生物相容性。
1 材料与方法 1.1 涂层的制备 1.1.1 热喷涂原料喷涂原料选用Nb2O5粉(上海杳田新材料科技有限公司,纯度>99.9%)、CuO粉(Aladdin,分析纯)和TiO2粉(P25,Degussa,德国)。按质量比为50∶50称取Nb2O5和TiO2粉,按质量比为1∶49∶50称取CuO、Nb2O5和TiO2粉,球磨4 h,使粉料充分混合。将混合充分的浆料置于鼓风干燥箱中干燥12 h,研磨烘干的粉料过80目筛,再向过筛后的粉末中添加适量浓度为5%的PVA溶液进行造粒烘干,最后研磨粉料依次过筛,去除细粉,取70~180 μm(80~200目)的粉末作为喷涂原料。采用相同方法制备TiO2喷涂粉。
1.1.2 涂层的制备采用尺寸为Ф10 mm×1 mm的钛合金(Ti-6Al-4V)作为涂层基体,喷涂前使用46号棕刚玉对基体进行喷砂处理。选用美国Sulzer Metco公司生产的9M型大气等离子喷涂设备制备涂层。喷涂工艺参数:氩气流量40 L/min,氢气流量12 L/min,喷涂功率42 kW,喷涂距离100 mm,送粉率20 g/min。
1.2 涂层的表征 1.2.1 涂层的微观形貌和结构表征采用X射线衍射仪(XRD,Rigaku,D/max 2500PC,日本)对涂层的物相组成进行表征。具体参数:Cu靶Kα辐射,特征波长λ=0.154 056 nm,衍射角(2θ)的扫描速度为0.02 (°)/s,扫描范围为 20°~80°,电流100 mA,电压40 kV。采用场发射扫描电子显微镜(FE-SEM,Zeiss,SUPRA55,德国)对涂层表面形貌进行观察。
1.2.2 涂层的表面粗糙度和表面润湿性表征采用手持式粗糙度仪(北京时代之峰科技有限公司,TR200)对涂层表面粗糙度进行测试。每个涂层样品表面随机选取10个点测量,取平均值。采用接触角测量仪(上海中晨数字技术设备有限公司,JC2000DI)测试涂层的水接触角,考察涂层的亲疏水性。每种涂层表面选取5个点测量,取平均值。
1.2.3 离子释放将涂层分别用无水乙醇和去离子水超声清洗后烘干,浸泡于20 mL的Tris-HCl缓冲溶液中,置于培养箱(36.5 ℃)中培养3、7和14 d。采用电感耦合等离子体发射光谱仪(Vista-Ax,Varian Company,America)测试浸泡液中含有涂层元素的离子浓度。
1.3 涂层的抗菌性能评价 1.3.1 细菌的培养利用革兰氏阳性菌金黄色葡萄球菌(S. aureus)和革兰氏阴性菌大肠杆菌(E. coli)对所制备的涂层的抗菌性能进行评价。首先,将金黄色葡萄球菌和大肠杆菌在琼脂培养板上,37 ℃培养箱中培养24 h后,用PBS稀释成108 CFU/mL的密度,然后用大豆肉汤培养基配制成密度107 CFU/mL的菌液备用。其次,将高温高压灭菌后样品置于24孔板中,每孔加入1 mL的细菌悬液,37 ℃下培养24 h。
1.3.2 细菌活性的评价将培养24 h后的样本用PBS清洗3次,然后每孔加入1 mL的MTT染色液(含0.5 mg/mL MTT的PBS溶液),将培养板放入培养箱中37 ℃培养1 h,然后将样品转移至新的24孔板中,每孔加入1 mL的二甲基亚砜(DMSO)溶液,室温避光环境下用摇床以80 r/min的速度摇晃20 min,将200 μL溶解有着色物质的DMSO溶液转移至 96孔板,用酶标仪测量波长在570 nm波长处的吸光度值。
1.3.3 菌落单位形成能力评价将培养24 h后的生物样本用PBS清洗3次后,将细菌从材料表面震荡下来,用PBS将细菌稀释104倍,然后取100 μL在琼脂板上涂匀,置于37 ℃的培养箱中培养24 h后,用菌落分析仪拍照和统计细菌的数量。
1.3.4 细菌形貌观察将培养24 h后的样本用PBS清洗3次,每孔加入1 mL 2.5%的戊二醛4 ℃固定过夜,去除戊二醛溶液,用PBS清洗3次后,依次用30%、50%、70%、80%、90%、95%和100%(体积分数)的乙醇逐级脱水10 min,干燥、喷铂后,用扫描电镜观察细菌形貌。
1.4 涂层的生物相容性评价 1.4.1 细胞的增殖将材料高温高压灭菌后置于24孔板中,用PBS清洗3次,将MC3T3-E1细胞以5×104 cells/孔的密度接种于材料上,在培养箱中分别培养1、3、5和7 d。在每个时间点,移除原培养液,每孔中加入500 μL的DMEM培养基(DMEM∶CCK-8=9∶1)后在培养箱中孵育2 h后,将收集液转移到96孔板中,每孔加入量为200 μL,用酶标仪测量在波长450 nm处的吸光度值,所有的试验重复3次。
1.4.2 碱性磷酸酶活性定量检测将材料高温高压灭菌后置于24孔板中,用PBS清洗3次,将MC3T3-E1细胞以5×104 cells/孔的密度接种材料上,在37 ℃,5% CO2的条件下分别培养3和 7 d后,按照碱性磷酸酶试剂盒的操作步骤来测量不同材料上碱性磷酸酶的含量。
1.4.3 与成骨相关基因的定量检测将材料高温高压灭菌后置于24孔板中,用PBS清洗3次,将MC3T3-E1细胞以1×105 cells/孔的密度接种材料上,在37 ℃,5% CO2的条件下培养14 d后,按照实时荧光定量PCR操作步骤来检测不同材料上与成骨相关基因Runx-2,OCN,OPN和ALP的表达。
2 结果与讨论 2.1 涂层的形貌和物相分析TiO2、50%Nb2O5-TiO2和1%CuO-49% Nb2O5-TiO2涂层的表面形貌如图1所示。所有的涂层均具有典型的等离子体喷涂涂层的表面形貌,由熔融、半熔融与少量未熔融颗粒组成,有些裂纹和气孔。从TiO2涂层的高倍图中可以看出,涂层表面由许多纳米颗粒构成,这些纳米颗粒的形成可能是由于熔融颗粒在等离子喷涂的快速固化过程中发生了重结晶。因等离子体喷涂具有超高温和超快速冷却两大特点,熔融颗粒在快速固化过程中,晶粒的生长会受到较大程度上的抑制,从而导致了涂层表面纳米晶粒的形成[21]。由于Nb2O5的掺入,在50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层表面形成了独有的棒状的特殊形貌。其中,1% CuO-49% Nb2O5-TiO2涂层表面的棒状形貌尺寸小于50% Nb2O5-TiO2涂层的,这可能是因为CuO的掺杂抑制了棒状晶粒的生长[22]。

|
| 图 1 TiO2、50% Nb2O5-TiO2和1%CuO-49% Nb2O5-TiO2涂层的表面形貌 Fig. 1 Surface morphologies of TiO2、50% Nb2O5-TiO2 and 1% CuO-49% Nb2O5-TiO2 coating |
TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2粉末和涂层的XRD图谱分析如图2所示。从图2看出,TiO2粉末主要是由锐钛矿相(TiO2, A)和少量的金红石相(TiO2, R)构成[23-24]。等离子体喷涂后,锐钛矿相向金红石相转变。在50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层中形成了Ti0.95Nb0.95O4固溶体,表明在喷涂过程中,Nb5+进入TiO2晶格中,形成了稳定的固溶体结构。

|
| 图 2 TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2粉末和涂层的XRD图谱 Fig. 2 XRD patterns of TiO2、50% Nb2O5-TiO2 and 1% CuO-49% Nb2O5-TiO2 powders and coatings |
TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层的表面粗糙度如图3(a)所示。从图中可以看出,涂层均具有微米级的表面粗糙度。TiO2涂层的表面粗糙度约为8 μm,掺入Nb2O5和CuO后,涂层的表面粗糙度逐渐升高。这可能是因为涂层表面形成了Ti0.95Nb0.95O4固溶体增加了涂层的表面粗糙度。

|
| 图 3 TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层的表面粗糙度和水接触角(*p<0.05; **p<0.01; ***p<0.001) Fig. 3 Surface roughness and water contact angle of TiO2、50% Nb2O5-TiO2 and 1% CuO-49% Nb2O5-TiO2 coating |
TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层表面的接触角如图3(b)所示。TiO2涂层的接触角大于90°,表现出疏水的性能,在掺入Nb2O5和CuO后,涂层表面的水接触角大幅度下降,1% CuO-49% Nb2O5-TiO2涂层的接触角最低,约为8°,亲水性能最优异。掺杂Nb2O5和CuO后涂层亲水性能的提高可能是因为在50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层表面形成了棒状的形貌,增加了涂层的表面粗糙度,有利于涂层表面水分子的扩散,从而提高了涂层的亲水性能[25]。因此,1% CuO-49% Nb2O5-TiO2涂层表面水接触角最小,表现出最好的亲水性。
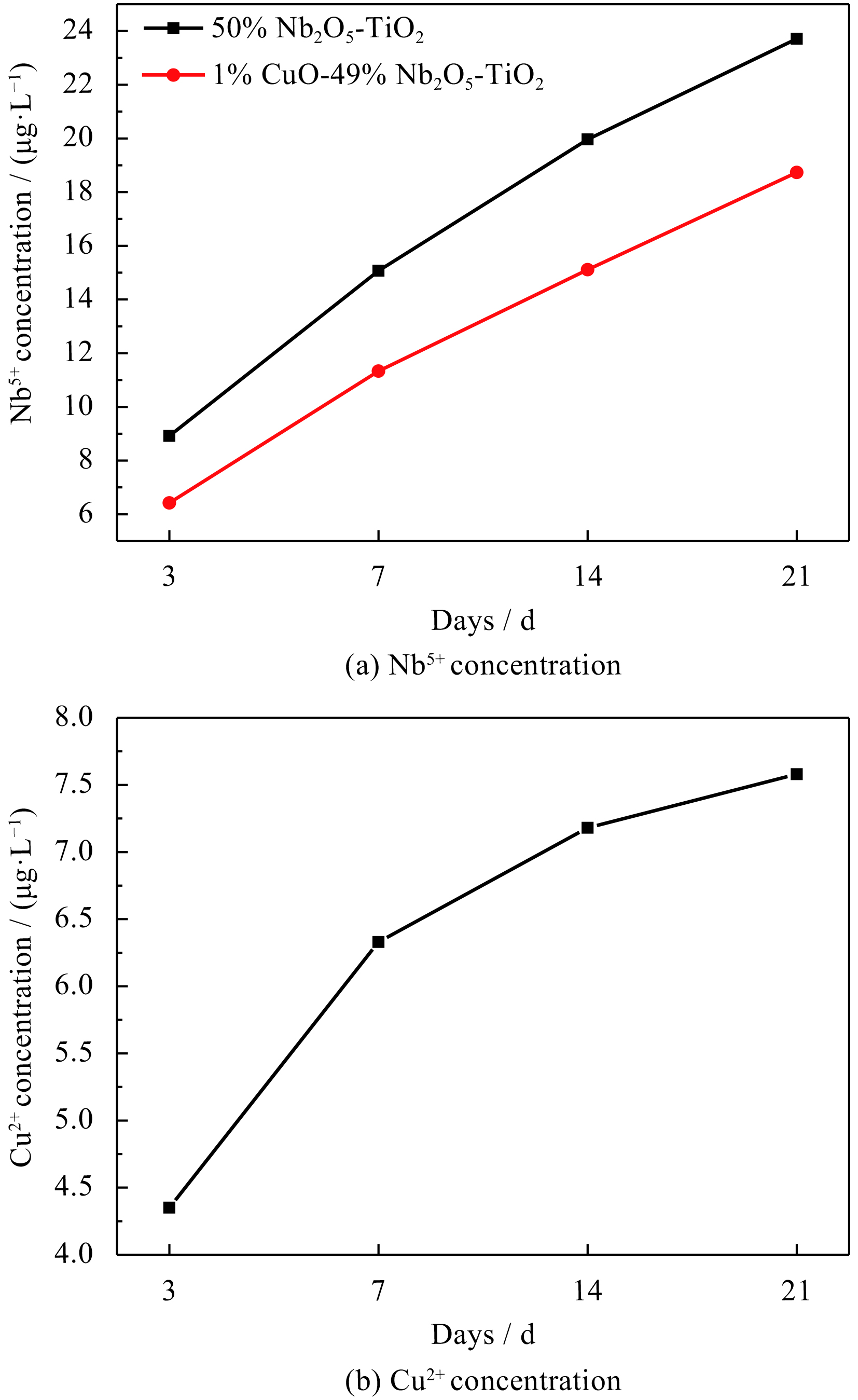
2.3 离子释放涂层在Tris-HCl缓冲溶液中的离子释放情况如图4所示。由于TiO2具有极好的化学稳定性,经过测试在浸泡后均未发现Ti4+的释放。图4(a)是50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层中Nb5+的释放情况,可以看出,随着浸泡天数的增加,Nb5+的释放量逐渐增多,但增加幅度逐渐减小,在21天后,50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层中Nb5+的释放量分别为24 μg/L和18 μg/L左右。图4(b)是1% CuO-49% Nb2O5-TiO2涂层中Cu2+的释放情况,从图中可知,随着浸泡时间的增加,Cu2+的释放幅度逐渐减少,在21天后达到了7.5 mg/L左右。可以发现,虽然涂层中CuO的掺杂量明显低于Nb2O5,但浸泡21天后Cu2+的释放量却达到了Nb5+释放量的416倍左右,这可能是由于Nb和Cu在晶格中处于不同位置导致的。
|
| 图 4 50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层浸泡在Tris-HCl溶液中的Nb5+和Cu2+的含量 Fig. 4 Content of Nb5+ and Cu2+ for 50% Nb2O5-TiO2 and 1% CuO-49% Nb2O5-TiO2 coating in Tris-HCl solution |
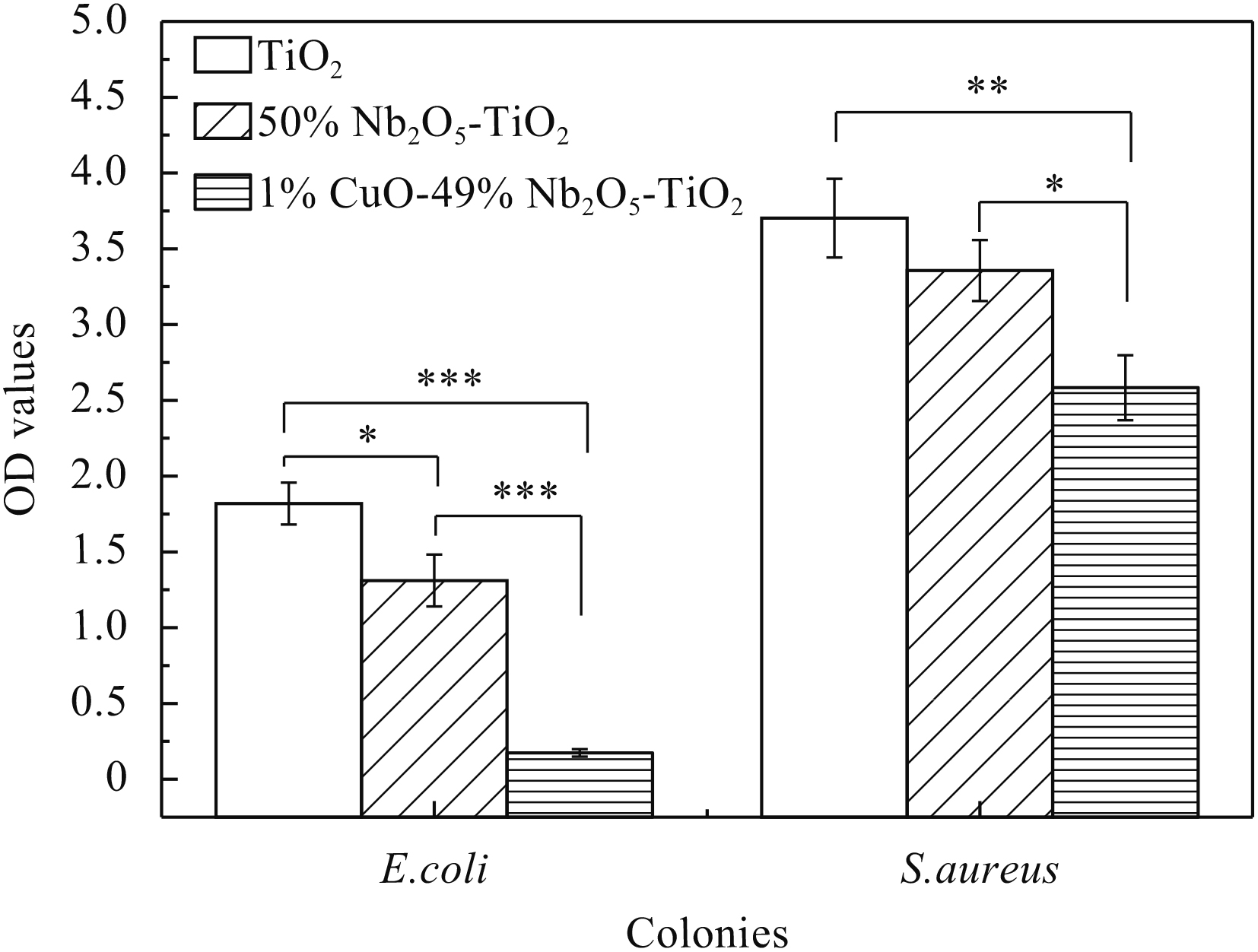
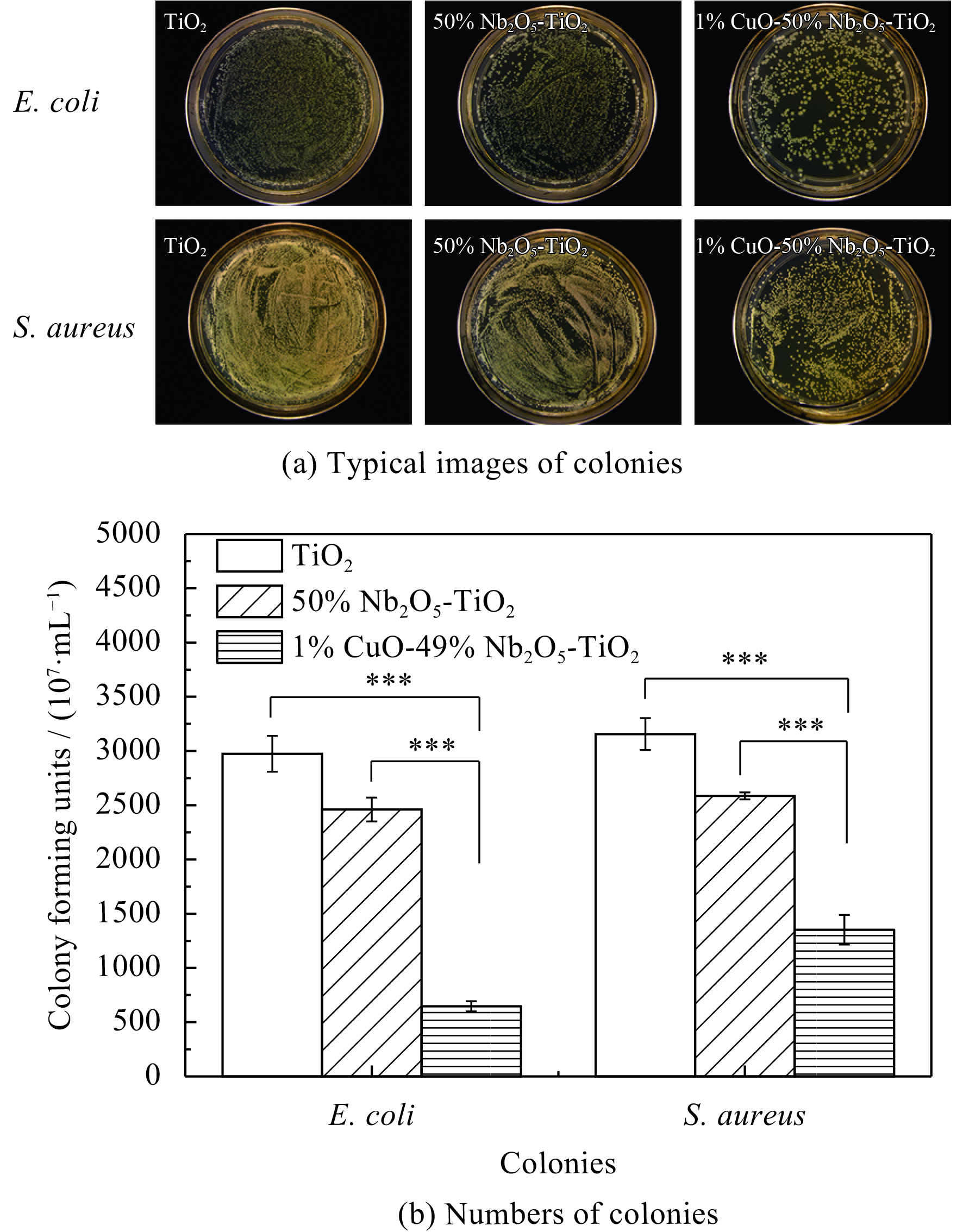
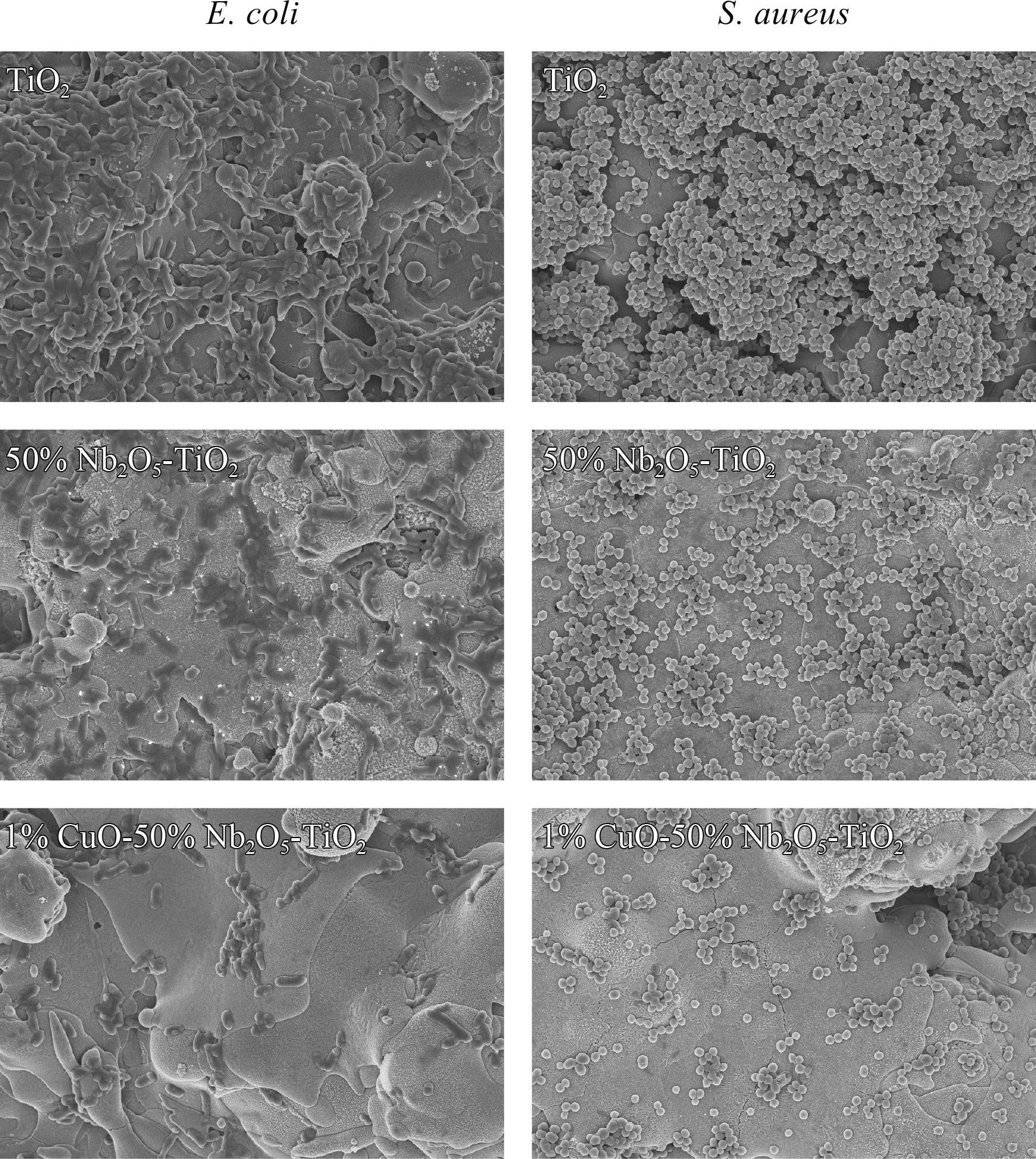
大肠杆菌(E. coli)和金黄色葡萄球菌(S. aureus)在TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2上的活性、菌落形成能力及细菌形貌分别见图5、图6和图7。从图5和图6可知,掺杂Nb2O5后,E. coli和S. aureus在50% Nb2O5-TiO2涂层上的生长受到一定的抑制。从图7可以发现,E. coli和S. aureus在50% Nb2O5-TiO2涂层上粘附的数量较少,部分细菌的细胞膜的完整性遭到破坏。这表明50% Nb2O5-TiO2涂层对E. coli和S. aureus具有微弱的杀伤作用,这可能是因为掺杂氧化铌后形成的特殊微纳米结构具有一定程度抑制细菌粘附的作用[26];但同时掺杂Nb2O5和CuO的涂层能够显著抑制E. coli和S. aureus的粘附(图5和6),且大部分细菌的细胞膜遭到破坏,使细菌丧失活性(图7)。综合此抗菌数据,可以得出如下结论:Nb2O5和CuO共同掺杂的涂层的抗菌性能最佳,其抗菌性能主要源自Cu离子的释放。Cu离子的抗菌性能已经被广泛报道,S. Wang等[27]人利用磁控溅射将Cu离子注入到纳米结构的钽基材上,并利用大肠杆菌和金黄色葡萄球菌验证材料的抗菌性能,研究结果表明,Cu离子的注入能够显著提高其抗菌性能。
|
| 图 5 TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层与E. coli和S. aureus培养24 h后的活性(*p<0.05; **p<0.01; ***p<0.001) Fig. 5 Bacterial activity of E. coli and S. aureus cultured on TiO2、50% Nb2O5-TiO2 and 1% CuO-49% Nb2O5-TiO2 for 24 h |
|
| 图 6 E. coli和S. aureus再培养24 h后在TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层上形成菌落的照片和细菌数量 (***p<0.001) Fig. 6 Typical images and numbers of re-cultivated E. coli and S. aureus colonies from samples after 24 h of incubation |
|
| 图 7 E. coli和S. aureus在TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层培养24 h后的SEM形貌 Fig. 7 SEM images of E. coli and S. aureus cultured on TiO2、50% Nb2O5-TiO2 and1% CuO-49% Nb2O5-TiO2 after incubation for 24 h |
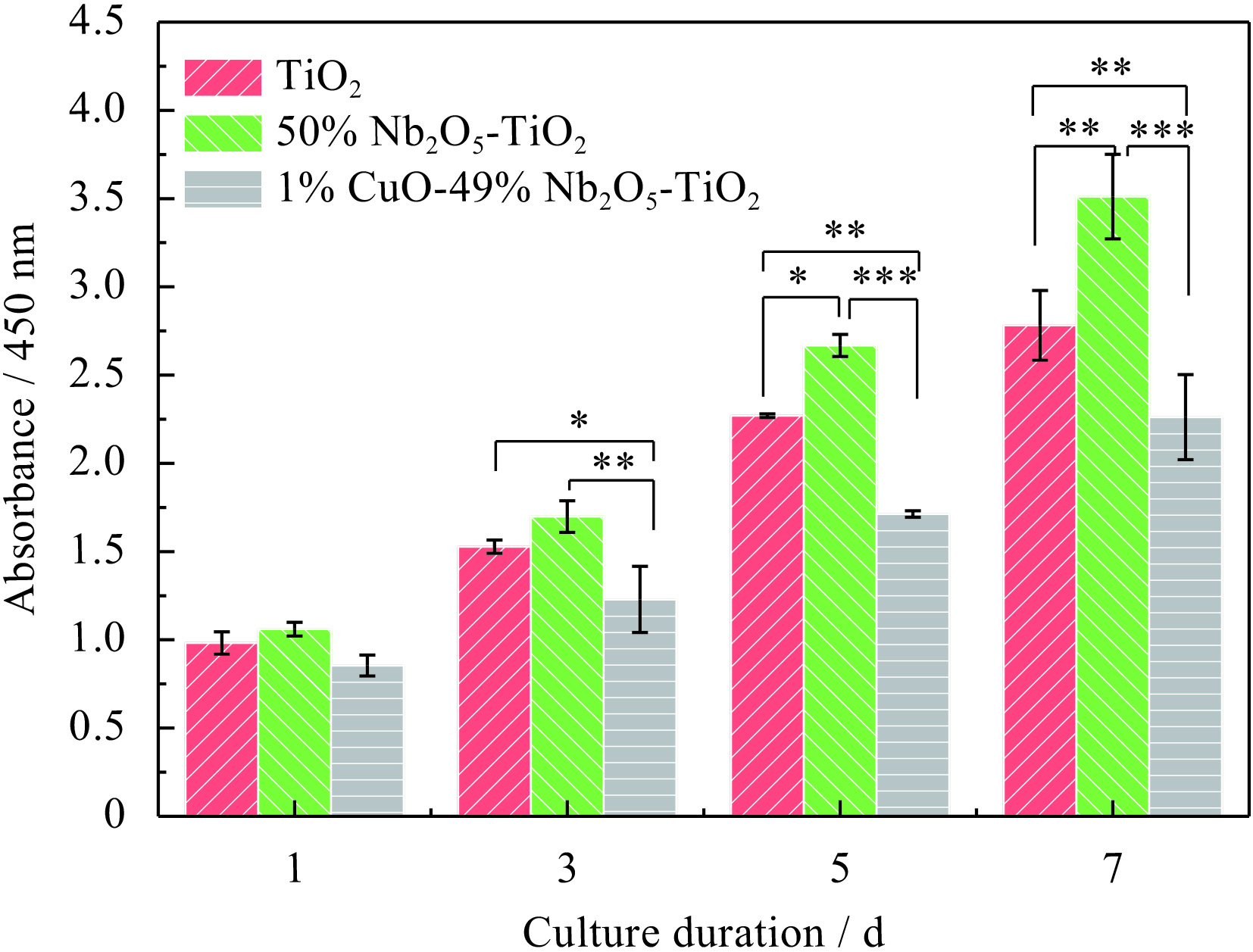
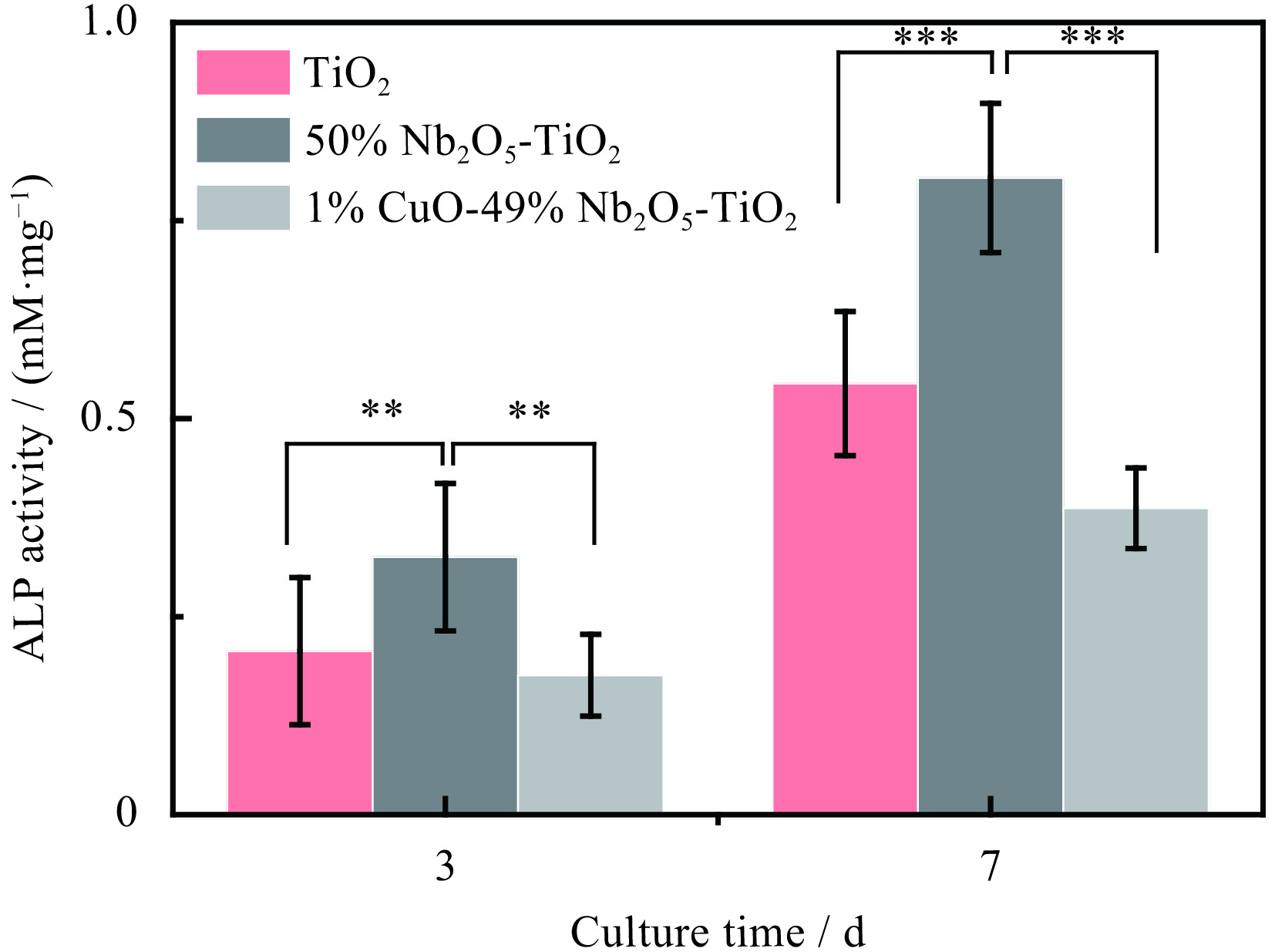
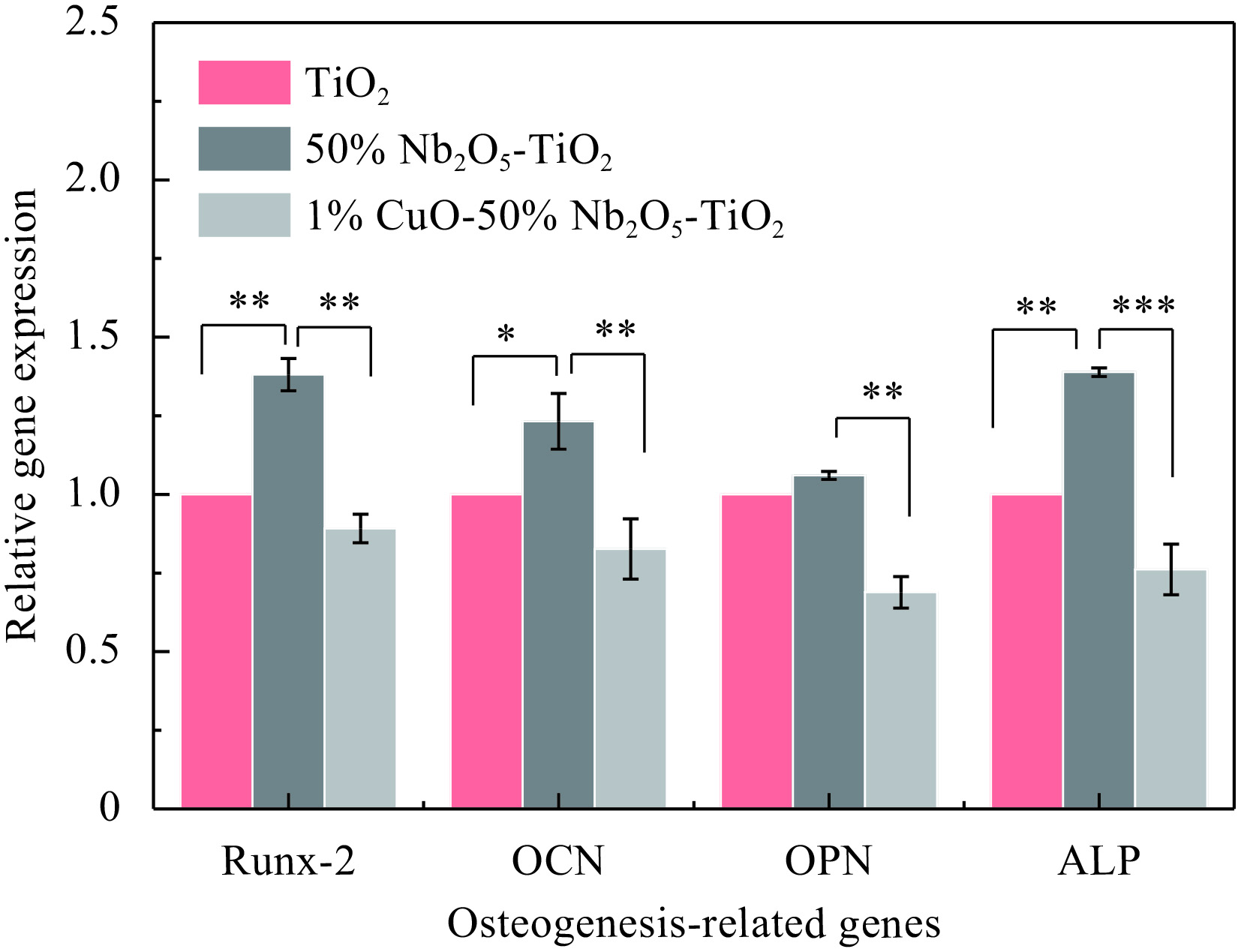
MC3T3-E1在TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2涂层上的增殖、碱性磷酸酶的活力及成骨相关基因的表达分别见图8~10。从图8中可知,随着培养时间的增加,MC3T3-E1在3种材料上均有增殖。在第5 d以后,MC3T3-E1在50% Nb2O5-TiO2上的增殖优于TiO2。从图9、10可知,Nb2O5掺杂不仅显著提高了细胞碱性磷酸酶的活性,同时上调了Runx-2、OCN、OPN和ALP的表达,此结果说明Nb2O5掺杂促进了细胞的成骨活性。从图3(b)可知,氧化铌掺杂提高了涂层的亲水性且导致特殊的微纳米结构的形成。据文献报道,细胞在亲水表面能够更好的粘附、增殖和成骨分化[28]。微纳米结构对成骨细胞功能的促进作用也得到了广泛验证。Jiang Shuai等的研究证明利用阳极氧化在钛合金表面形成的微纳米结构能够显著促进骨整合[29]。因此,认为良好的亲水性和微纳米结构是50% Nb2O5-TiO2涂层具有较好生物活性的主要原因。CuO掺杂后,不论是碱性磷酸酶活性还是成骨基因表达较单纯的Nb2O5掺杂都有明显减弱,但和TiO2涂层相比减弱并不是十分明显,这说明Nb2O5的掺杂一定程度上缓解了Cu离子释放造成的副作用。
|
| 图 8 TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2与MC3T3-E1分别培养1、3、5和7天后的增殖(*p<0.05; **p<0.01; ***p<0.001) Fig. 8 Cell proliferation of MC3T3-E1 cultured on TiO2、50% Nb2O5-TiO2 and 1% CuO-49% Nb2O5-TiO2 for 1, 3, 5 and 7d, respectively |
|
| 图 9 TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2与MC3T3-E1分别培养3 d和7 d后的碱性磷酸酶的活性(**p<0.01; ***p<0.001) Fig. 9 ALP activity of the MC3T3-E1 cultured on TiO2、50% Nb2O5-TiO2 and 1% CuO-49% Nb2O5-TiO2 for 3 and 7 d |
|
| 图 10 TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5-TiO2与MC3T3-E1培养14 d后与成骨相关基因的表达(*p<0.05; **p<0.01; ***p<0.001) Fig. 10 Real-time PCR detection of osteogenesis-related genes expressed by the MC3T3-E1 cultured on TiO2、50% Nb2O5-TiO2 and 1% CuO-49% Nb2O5-TiO2 for 14 d |
利用等离子体喷涂技术在钛合金表面制备了TiO2、50% Nb2O5-TiO2和1% CuO-49% Nb2O5 -TiO2涂层,研究了Nb2O5和CuO共掺对TiO2涂层生物活性和抗菌性能的影响。结果表明:Nb2O5和CuO掺杂提高了TiO2涂层的表面粗糙度、亲水性。Nb2O5掺杂可显著提高成骨细胞的增殖和成骨活性,CuO和Nb2O5共掺杂的涂层具有显著的抗菌性能,但Cu离子的释放一定程度上降低了涂层表面细胞的活性。此结果证明Nb2O5掺杂一定程度上可降低Cu离子对细胞的负面作用。
| [1] | GEETHA M, SINGH A K, ASOKAM A R, et al. Ti based biomaterials, the ultimate choice for orthopaedic implants - A review[J]. Progress in Materials Science, 2009, 54(3): 397-425. |
| 点击浏览原文 | |
| [2] | NIINOMI M. Mechanical biocompatibilities of titanium alloys for biomedical applications[J]. Journal of the Mechanical Behavior of Biomedical Materials, 2008, 1(1): 30-42. |
| 点击浏览原文 | |
| [3] | PULEO D A, KISSLING R A, SHEU M S. A technique to immobilize bioactive proteins, including bone morphogenetic protein-4(BMP-4), on titanium alloy[J]. Biomaterials, 2002, 23(9): 2079-2087. |
| 点击浏览原文 | |
| [4] | CIOFFI M, GILLILAND D, CECCONE G, et al. Electrochemical release testing of nickel-titanium orthodontic wires in artificial saliva using thin layer activation[J]. Acta Biomaterialia, 2005, 1(6): 717-724. |
| 点击浏览原文 | |
| [5] | LONG M, RACK H J. Titanium alloys in total joint replacement--A materials science perspective[J]. Biomaterials, 1998, 19(18): 1621-1639. |
| 点击浏览原文 | |
| [6] | LIU X, DING C. Plasma sprayed wollastonite/TiO2 composite coatings on titanium alloys[J]. Biomaterials, 2002, 23(20): 4065-4077. |
| 点击浏览原文 | |
| [7] | LYU C, XU Z J, LU H F, et al. Modulation of the micro/nanotopography of plasma sprayed biomedical coatings for enhanced osteogenic activity[J]. Surface Review and Letters, 2018: 1950061. |
| 点击浏览原文 | |
| [8] | MEI S Li, WANG H Y, CHU P K, et al. Antibacterial effects and biocompatibility of titanium surfaces with graded silver incorporation in titania nanotubes[J]. Biomaterials, 2014, 35(14): 4255-4265. |
| 点击浏览原文 | |
| [9] | COCHIS A, AZZIMON B T, DELLA C V, et al. The effect of silver or gallium doped titanium against the multidrug resistant Acinetobacter baumannii[J]. Biomaterials, 2016, 80: 80-95. |
| 点击浏览原文 | |
| [10] | ZHOU L, LAI Y Z, HUANG W X, et al. Biofunctionalization of microgroove titanium surfaces with an antimicrobial peptide to enhance their bactericidal activity and cytocompatibility[J]. Colloids and Surfaces B: Biointerfaces, 2015, 128: 552-560. |
| 点击浏览原文 | |
| [11] | NARBAT M K, KINDRACHUK J, DUAN K, et al. Antimicrobial peptides on calcium phosphate-coated titanium for the prevention of implant-associated infections[J]. Biomaterials, 2010, 31(36): 9519-9526. |
| 点击浏览原文 | |
| [12] | MARIA G G, CARLOS M M, MARA C F C, et al. Covalent immobilization of hLf1-11 peptide on a titanium surface reduces bacterial adhesion and biofilm formation[J]. Acta Biomaterialia, 2014, 10(8): 3522-3534. |
| 点击浏览原文 | |
| [13] | LV H B, CHEN Z, YANG X P, et al. Layer-by-layer self-assembly of minocycline loaded chitosan/alginate multilayer on titanium substrates to inhibit biofilm formation[J]. Journal of Dentistry, 2014, 42(11): 1464-1472. |
| 点击浏览原文 | |
| [14] | ZHANG F, ZHANG Z, ZHU X, et al. Silk-functionalized titanium surfaces for enhancing osteoblast functions and reducing bacterial adhesion[J]. Biomaterials, 2008, 29(36): 4751-4759. |
| 点击浏览原文 | |
| [15] | MEHDI K N, BENJAMIN F L, DING C F, et al. Multilayered coating on titanium for controlled release of antimicrobial peptides for the prevention of implant-associated infections[J]. Biomaterials, 2013, 34(24): 5969-5977. |
| 点击浏览原文 | |
| [16] | YAO X H, ZHANG X Y, WU H B, et al. Microstructure and antibacterial properties of Cu-doped TiO2 coating on titanium by micro-arc oxidation[J]. Applied Surface Science, 2014, 292: 944-947. |
| 点击浏览原文 | |
| [17] | FINNEY L, VOGT S, FUKAI T, et al. Copper and angiogenesis: Unravelling a relationship key to cancer progression[J]. Clinical and Experimental Pharmacology and Physiology, 2010, 36(1): 88-94. |
| [18] | WU Q J, LI J H, ZHANG W J, et al. Antibacterial property, angiogenic and osteogenic activity of Cu-incorporated TiO2 coating[J]. Journal of Materials Chemistry B, 2014(2): 6738-6749. |
| 点击浏览原文 | |
| [19] | HEIDENAU F, MITTELMEIER W, DETSCH R, et al. A novel antibacterial titania coating: Metal ion toxicity and in vitro surface colonization[J]. Journal of Materials Science: Materials in Medicine, 2005, 16(10): 883-888. |
| 点击浏览原文 | |
| [20] | ZHANG L, GUO J Q, HUANG X Y, et al. The dual function of Cu-doped TiO2 coatings on titanium for application in percutaneous implants[J]. Journal of Materials Chemistry B, 2016, 4(21): 3788-3800. |
| 点击浏览原文 | |
| [21] | LI F X, LU X H, MEI P. Progress in research on effects of metal ion dopants on crystal phase transformation of TiO2[J]. Materials Review, 2006, 20(9): 13-16. |
| 点击浏览原文 | |
| [22] | LI Y P, XU X W, WANG B, et al. Research on the fluxed effect of LiF and B2O3[J]. Journal of University of Science & Technology Beijing, 2002, 24(4): 429-431. |
| 点击浏览原文 | |
| [23] | YANG G J, LI C J, HAN F, et al. Microstructure and photocatalytic performance of high velocity oxy-fuel sprayed TiO2 coatings[J]. Thin Solid Films, 2004, 466(1-2): 81-85. |
| 点击浏览原文 | |
| [24] | TOKI S M O. Fabrication and properties of TiO2 photo-catalytic coatings by thermal spraying with TiO2-Al agglomerated powder[J]. Journal of High Temperature Society, 2001, 27(4): 274-279. |
| [25] | LI G S, JIN M F, WEI G, et al. On wettability of binding phase in fluorine-bearing sinter[J]. Iron & Steel, 2007, 42(8): 12-16. |
| 点击浏览原文 | |
| [26] | YAO C, WEBSTER T J, HEDRICK M. Decreased bacteria density on nanostructured polyurethane[J]. Journal of Biomedical Materials Research Part A, 2014, 102(6): 1823-1828. |
| 点击浏览原文 | |
| [27] | WANG S, ZHU W, YU P, et al. Antibacterial nanostructured copper coatings deposited on tantalum by magnetron sputtering[J]. Materials & Processing Report, 2015, 30(6): B120-B125. |
| 点击浏览原文 | |
| [28] | YOSHINARI M, ODA Y, KATO T, et al. Influence of surface modifications to titanium on oral bacterial adhesion in vitro[J]. Journal of Biomedical Materials Research Part A, 2015, 52(2): 388-394. |
| [29] | LI X, XU H, ZHAO B, et al. Accelerated and enhanced osteointegration of MAO-treated implants: histological and histomorphometric evaluation in a rabbit model[J]. International Journal of Oral Science, 2018, 10(2): 21-31. |
| 点击浏览原文 |



