2. 佳木斯大学 机械工程学院,黑龙江 佳木斯 154007;
3. 哈尔滨焊接研究院有限公司,哈尔滨 150000
2. College of Mechanical Engineering, Jiamusi University, Jiamusi 154007, Heilongjiang;
3. Harbin Welding Institute Limited Company, Harbin 150000
镁及其合金由于其可降解性成为国内外生物医用材料研究的重点。但镁的电位低,在植入人体中极易发生电化学腐蚀,体内降解速率过快,在皮下产生的氢气超过人体的吸收范围,作为骨内固定材料不能满足临床应用的需求。因此,如何控制其腐蚀速率是研究的重点[1-2]。
目前,对镁及其合金进行微弧氧化处理和硅烷转化膜处理能够有效提高表面的耐蚀性。微弧氧化电击穿表面产生的瞬时高温,使镁表面形成多孔的陶瓷层,其厚度可控,耐蚀性和耐磨性能优异[3-4],但膜层仍有贯穿孔隙和裂纹存在[5-6]。硅烷偶联剂是一种能与有机和无机膜层发生作用的特殊有机化合物,在防止金属表面腐蚀有着广泛的应用[7-8]。表面硅烷化处理是金属防腐领域一种新型的环保、节能、低排放、低成本的处理技术,可提高镁合金耐腐蚀性[9-10]。Córdoba和Chen等[11-12]在基体表面制备了硅烷膜,并掺杂其他物质,都使基体的耐蚀性有了很大的提高。硅烷与金属偶联的机理为硅烷水解成硅醇,硅醇缩聚形成−Si−O−骨架,游离的羟基与金属表面碱处理的羟基形成氢键,最后固化脱水形成稳定的共价键[13-14],但多数还是用于镁合金表面单一处理,长期的有效性还待提高。通过在硅烷中添加纳米粒子可使其耐腐蚀性能有所提高[15-16]。
作为骨内固定材料,植入体的感染一直是临床上棘手问题[17]。在植入体植入的早期,细菌容易在材料表面形成菌膜,产生大量菌落,导致炎症的发生。因此,植入体表面抗菌的特性是植入成功的主要因素之一[18-19]。葛根为豆科植物野葛的干燥根,是中国传统中药,具有极高的营养价值和医药价值[20-21],葛根素是从豆科植物野葛的根中提取的有效成分,主要化学成分为黄酮类化合物葛根黄酮,分子式为C21H20O9[22-23],在临床应用中主要剂型有片剂、注射剂等,具有抗炎、提高免疫促进成骨细胞增殖和减少骨质疏松发生的概率[24-25]。能否将中药提取物葛根素引入纯镁膜层,促进骨生长,并赋予表面抗菌性少见报道。课题组以多巴胺为偶联剂,将葛根素引入钛微弧氧化膜层中,抗菌率达到99.9%,并促进成骨细胞的黏附、增殖、分化及碱性磷酸酶表达[26]。
综上所述,针对医用可降解镁及其合金的腐蚀速率过快和临床感染问题,课题组提出将中药提取物葛根素引入纯镁膜层,赋予可降解医用纯镁表面功能化的设计思想。采用超声波技术与微弧氧化技术复合[27],使纯镁表面形成内致密外多孔膜层;在硅烷偶联剂中添加中药提取物葛根素,使硅烷水解液形成含有不同粒子复合浸渍液,弥合到超声微弧氧化贯穿孔隙和表面,使膜内掺入不同浓度葛根素,进而解决微弧氧化贯穿孔造成体液侵蚀镁基体的问题,并通过掺入葛根素提高了膜层的生物性能,并已申报发明专利[28]。因此,在前期试验研究的基础上,文中主要考察硅烷偶联剂中添加不同浓度的葛根素,形成复合膜层对耐蚀性和体外生物活性的影响。为将我国中药瑰宝引入到生物材料中,实现促进骨生长,并赋予UMAO(Ultrasonic micro arc oxidation,UMAO)涂层抗菌性功能,加快可降解镁在临床骨内固定的应用,提供理论研究基础。
1 试验与方法 1.1 样品制备试验采用的是99.9 %的纯镁,线切割加工成10 mm×10 mm和15 mm×15 mm的镁片,依次用500、1 000、2 000号的砂纸打磨,放入酒精中超声清洗。用质量分数10% H3PO4和120 g/L的NaOH依次分别处理30 s,最后用蒸馏水清洗,达到去油的目的。
微弧氧化电源为双极型脉冲电源(哈尔滨工业大学生产),电压为300 V,脉宽为50 μs,频率为500 Hz,时间为10 min,超声波的频率为60 kHz,超声功率为50 W。超声微弧氧化后的镁片用蒸馏水清洗,并悬挂阴干。再将UMAO的镁片置于120 g/L的NaOH溶液中碱处理1 h后用蒸馏水冲洗阴干。配置硅烷溶液,酒精:水:硅烷(KH-550)体积比为9∶1∶1,用氨水将pH调到8~9之间,沉化24 h备用。取配好的硅烷水解液,按载药浓度为1.2 mg/mL、2.0 mg/mL配得硅烷载药溶液。将超声微弧氧化碱处理的镁片浸渍硅烷溶液中30 s,甩干,重复3次,晾干,经过80 ℃下固化,得到膜层为硅烷(Silane coupling agent,SCA)膜。按浸渍硅烷液的方法浸渍不同浓度硅烷载药溶液得到载药为1.2 mg/mL膜层、载药为2.0 mg/mL的膜层。
1.2 表征与分析采用带FALCON60S能谱分析仪(EDAX)的JSM-6360LV扫描电子显微镜(SEM)分析观察膜层表面形貌和元素分布;使用德国Brooke Corporation制造的D8-ADVANCE型X射线衍射仪(XRD),Cu靶,初始角度为小角度2°,扫描速度2θ为10°/min;使用VECTOR33型傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)在分辨精度为4 cm−1,扫描波长为400~4 000 cm−1的条件下,对从膜层表面轻刮下并与KBr混合的粉末,进行官能团检测;采用JC2000C1型接触测量仪测定膜层表面接触角,在试样表面滴0.5 mL的蒸馏水,用摄像机拍摄稳定后的液滴,对图像用量角法获得润湿角数值。
使用德国制造的IM6e Princeton 400电化学工作站测定不同载药膜层的电化学腐蚀曲线和阻抗。测试试样作为工作电极,铂片作为辅助电极,用饱和甘汞电极作为参比电极。电化学测试溶液为9 g/L氯化钠溶液生理盐水,有效暴露面积1 cm2,扫描速度0.5 mV/s;模拟体液(Simulated body fluid,SBF)配方为日本Kukobo研究组研制,用盐酸与三羟甲基氨基甲烷调节pH至7.4,与人体体液的pH值相符,模拟体液浸泡温度保持在(37±0.5) ℃下,浸泡时间为7 d和11 d,并对表面进行SEM观察、主要元素测定和XRD相分析,研究其体外生物活性。
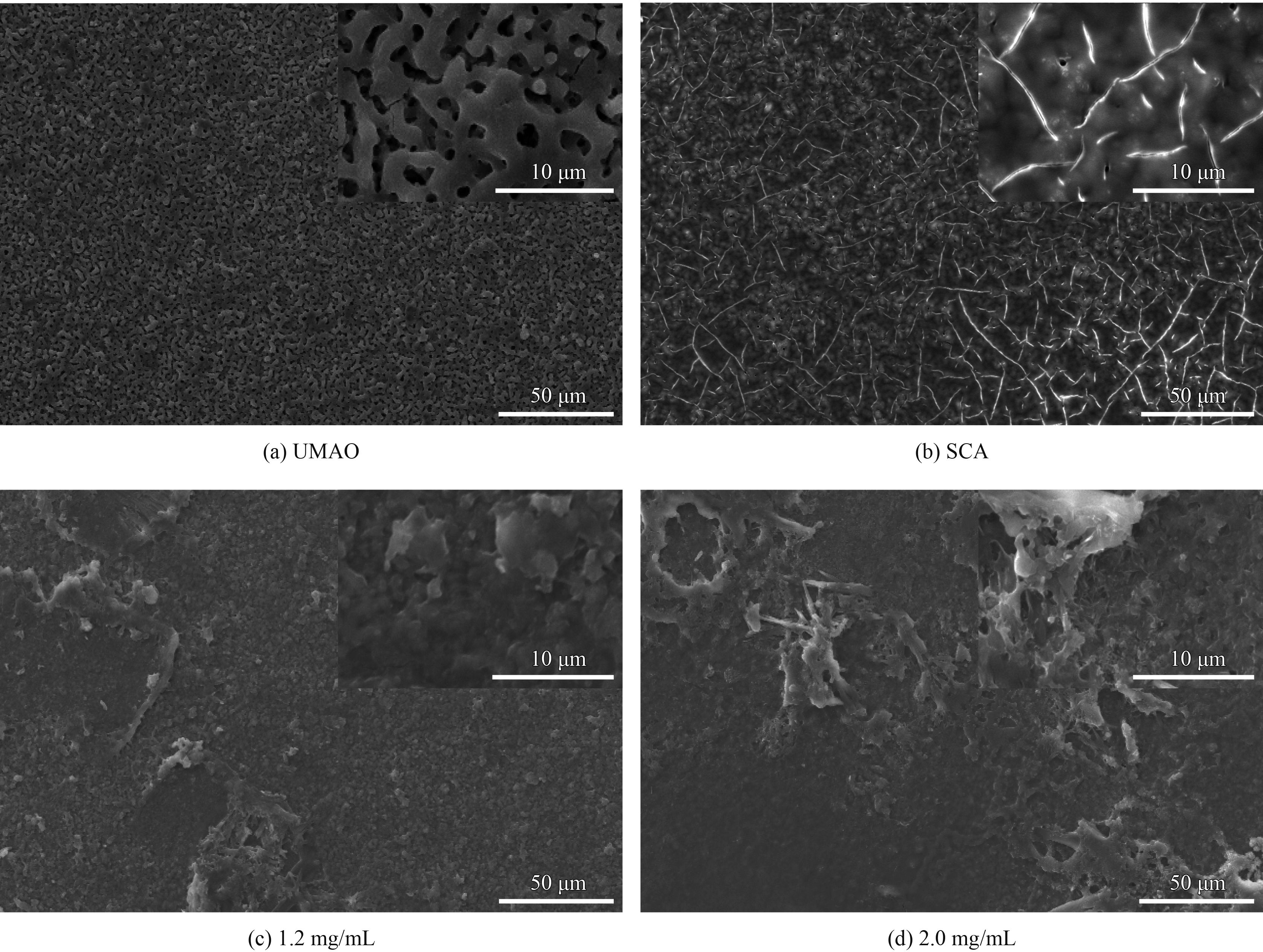
2 结果与讨论 2.1 膜层的表面形貌和元素分布载不同浓度葛根素膜层表面的SEM形貌和元素分布见图1。观察纯Mg的UMAO膜层(图1(a)),低倍下其表面分布微孔,高倍下分布着由大量高低不平小孔组成的交织网状结构;UMAO膜层经过硅烷浸渍后(图1(b)),其表面的孔洞被硅烷封住,形成阻挡层,但有白色龟裂条纹产生,这可能是微弧氧化膜层表面浸渍SCA膜层过厚造成,干燥后膜层表面产生拉应力,造成龟裂;在高倍下依然有微孔出现;图1(c)(d)分别为载药1.2 mg/mL和2 mg/mL膜层的形貌,其空隙被填满,有的孔被完全覆盖,但高倍下依然为凸凹不平的表面,随着葛根素浓度增加表面变得不均匀。
|
| 图 1 载不同浓度葛根素膜层的表面形貌 Figure 1 Surface morphologies of coatings with puerarin under different concentration |
制备UMAO膜层的硅酸盐镀液主要元素为Mg、O、Si,并有少量的F、Na、K元素(图2(a))。当表面浸渍硅烷后,Si含量增加,并有新元素N、C产生(图2(b))。这主要是由于硅烷中含有Si、N、C元素。当硅烷中添加葛根素时,与纯SCA膜层相比C和O元素的含量增加,这是由于葛根素是植物根提取物,主要是由C、H、O元素构成(图2(c)(d))。
微弧氧化生成陶瓷层(图1(a)),再碱处理使表面附着羟基,硅烷水解生成的硅醇与UMAO膜层表面羟基形成氢键,依靠毛细作用浸入孔隙中,80 ℃下固化,硅醇与贯穿孔隙裸露的基体Mg脱水形成−Si−O−Mg−愈合了裂纹和孔隙,形成具有耐蚀性的膜层(图1(b));掺杂醇溶解的葛根素稀释了硅烷液,浸泡中与硅烷水解液中游离的−OH形成氢键或包裹在硅醇缩合的−Si−O−Si−骨架中,形成一层载葛根素复合膜层(图1(c)(d))。

|
| 图 2 载不同浓度葛根素膜层元素含量 Figure 2 Element content of coatings with puerarin under different concentration |
图3为载不同浓度葛根素膜层的FTIR图。对于UMAO组在580 cm−1左右处为强的Mg−O吸收峰,900~1 100 cm−1为
当浸渍硅烷后在910 cm−1左右出现Si−OH振动峰,在1 020~1 090 cm−1出现强而宽的吸收峰,这是由于硅烷Si−O−Si骨架的振动而产生的。当在硅烷水解液中添加葛根素时,有新峰出现在1 450 cm−1和977 cm−1处,分别为苯环骨架弯曲振动和苯环中−C−H−的弯曲振动峰,葛根素含有苯环,说明被载入膜层中。
另外,载葛根素膜层在910 cm−1左右出现Si−OH振动减弱,这是由于葛根素的加入与硅烷水解的羟基发生键合,使游离Si−OH减少,导致吸收峰下降,但在1 020~1 090 cm−1依然有硅烷骨架吸收峰存在。各种膜层在1 639 cm−1、3 450 cm−1为结晶H2O和−OH吸收峰,2 860 cm−1、2 934 cm−1为硅烷和葛根素中−C−H−的不对称伸缩振动。

|
| 图 3 载不同浓度葛根素膜层的FTIR Figure 3 FTIR of coatings with puerarin under different concentrations |
图4显示的是载不同浓度葛根素膜层的润湿角。UMAO的润湿角为9.38°,亲水性优异。硅烷浸渍后,润湿角为52.71°,随着载药浓度的增加,润湿角增加,但均小于90°,说明亲水性减弱。浸渍硅烷和载葛根素膜层,硅烷骨架相互交互,使膜层更加致密,这相对于单纯的多孔微弧氧化表面来说,减少了体液与表面的接触面积,接触角变大,有可能减缓了人体体液向膜层的渗入,提高了镁表面的耐蚀性。

|
| 图 4 载不同浓度葛根素膜层的润湿角 Figure 4 Contact angles of coatings with puerarin under different concentrations |
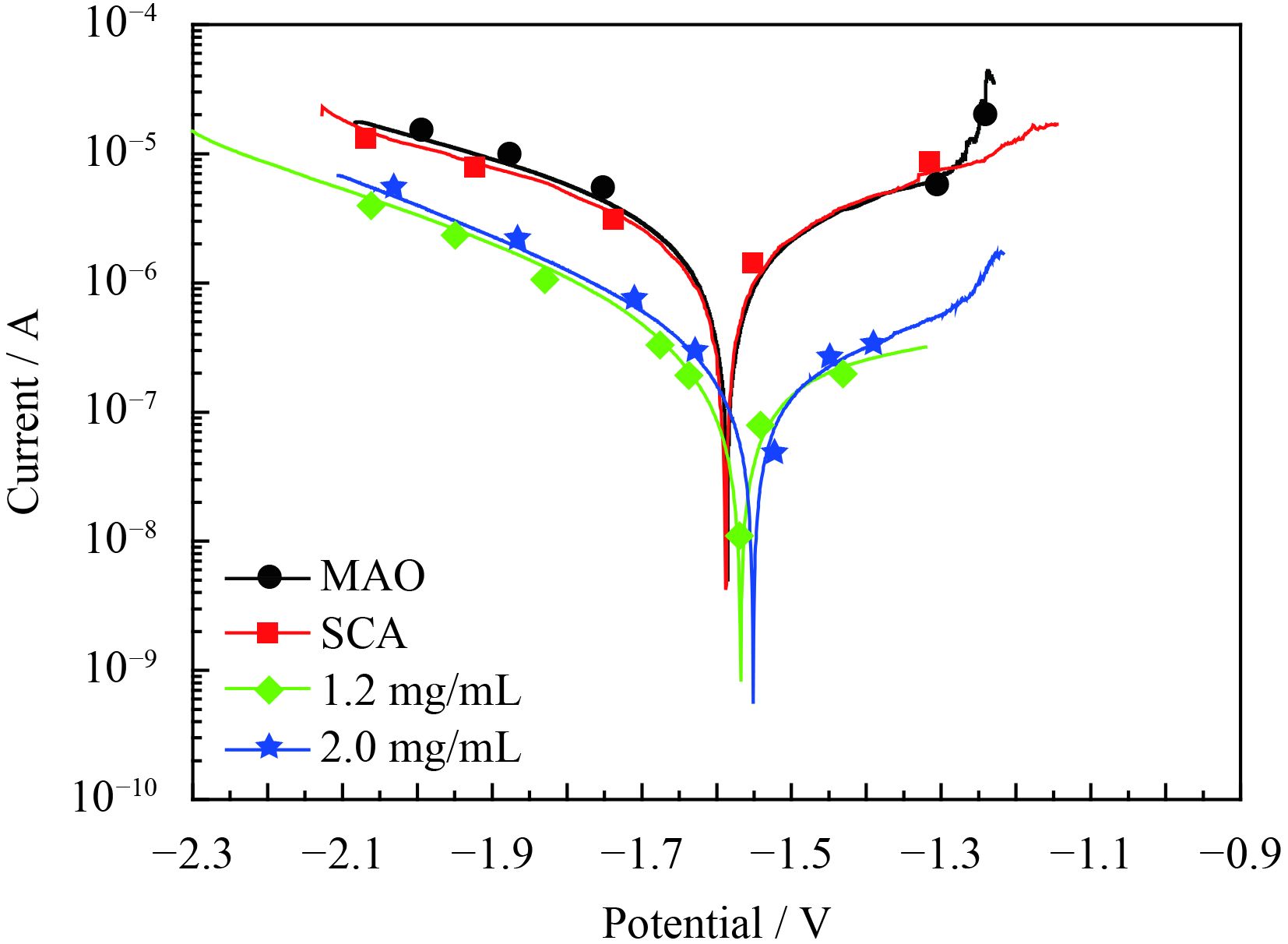
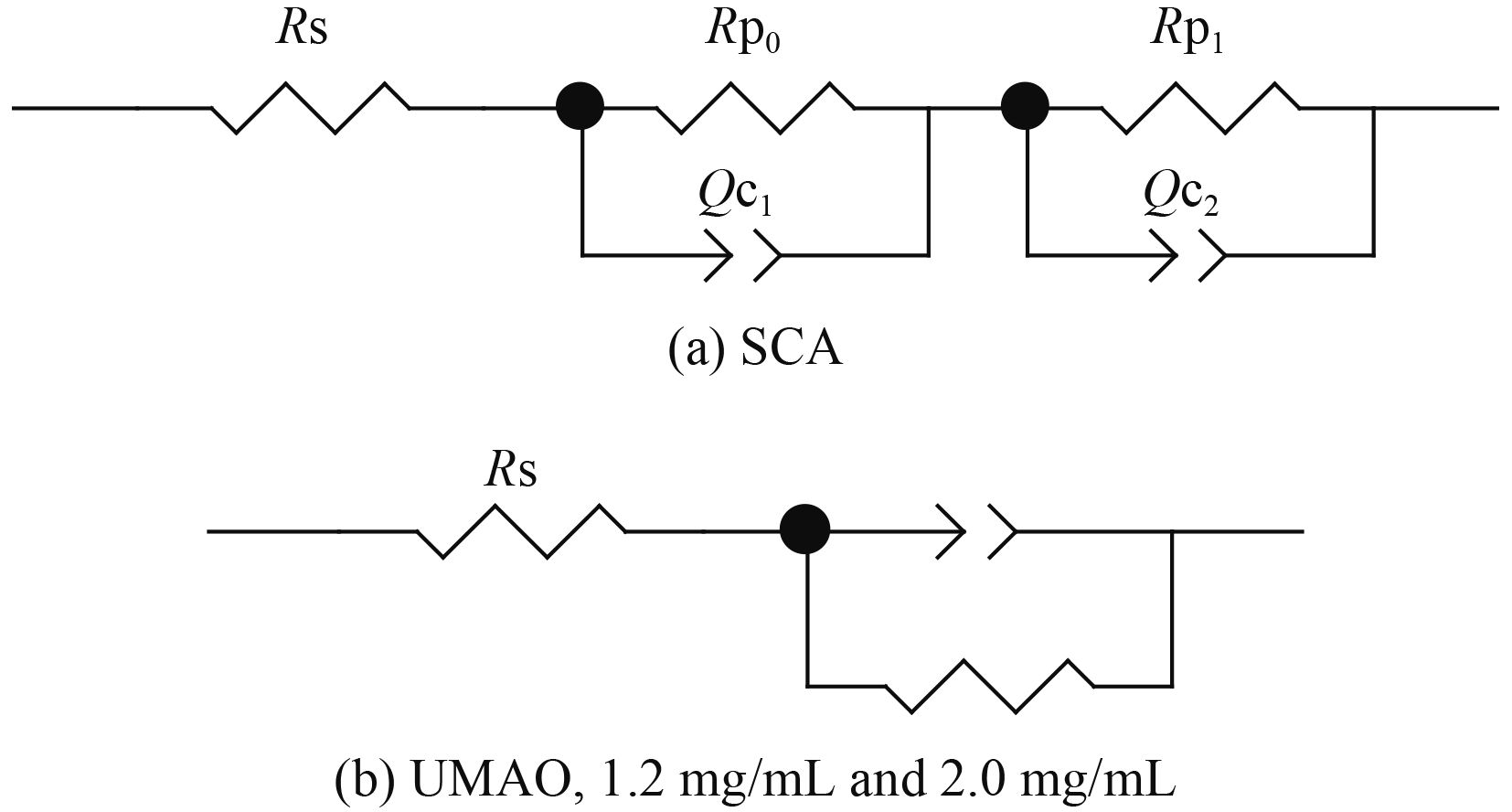
图5是载不同浓度葛根素膜层的极化曲线,可知相对于UMAO,随着载药浓度的增加,SCA膜层的自腐蚀电位略右移,1.2 mg/mL,2 mg/mL的电位分别提高20 mV和40 mV,自腐蚀电流逐渐下降,载葛根素的两组自腐蚀电流降低了1个数量级。图6是由软件Zview拟合的膜层阻抗等效电路模型,图7是载不同浓度葛根素膜层的阻抗和相应软件Zview拟合的阻抗,表1为载不同浓度葛根素膜层的电化学参数。其中图6和表1的Rs代表溶液电阻,Rp0代表孔内溶液电阻,Qc1代表膜层的容抗,而对于SCA组,Qc2为SCA层与微弧氧化层的双电层电容,Rp1为微弧氧化表面腐蚀反应的极化电阻。可知载药膜层阻抗是单纯微弧氧化的9~10倍,是SCA膜层的3~4倍。由此可见,在硅烷中掺杂葛根素,随着葛根素的含量增加,膜层自腐蚀电流下降,阻抗升高。
|
| 图 5 载不同浓度葛根素膜层的极化曲线 Figure 5 Polarization curves of coatings with puerarin under different concentrations |
电化学腐蚀试验中当试样浸泡到0.9%NaCl中,膜层与溶液会形成一个界面电容,遇到不同的相就会形成一个新的界面电容。镁表面上的硅烷载药膜层是一种无机与有机的复合膜层,外表面主要是有机层,能够延缓NaCl溶液渗入镁基体表面,降低了膜层的腐蚀速率。在做阻抗以及极化曲线试验时,膜层在NaCl溶液中处于浸泡初期,膜层的耐渗水性对镁的腐蚀速率影响很大。
图6(a)为SCA组的阻抗等效电路模型,为两个时间常数的EIS等效电路,这说明在浸泡初期NaCl溶液均匀的渗入到SCA层和微弧氧化层之间。图6(b)为UMAO,1.2 mg/mL, 2 mg/mL的等效电路模型。浸泡初期,对于UMAO膜层,NaCl溶液还未渗透到镁基体。对于载药组,其形成的界面电容是掺杂葛根素形成的硅烷阻挡层与腐蚀溶液形成的。载药后的膜层阻抗增加,说明单纯在镁超声微弧氧化表面浸渍的SCA膜层不能最有效的提高耐蚀性。
|
| 图 6 膜层阻抗的等效模型 Figure 6 Equivalent circuit model of coatings |
从润湿角分析来说,硅烷组与载药组的接触角相差并不大,阻碍水的渗入能力基本相同,但电化学腐蚀试验表明添加药物之后阻抗大大提高,这可能是由于交联在硅烷骨架之中的葛根素分子起到了进一步封孔作用,能够阻碍Cl−的进入,减缓膜层的腐蚀,防止了盐水浸入镁基体。硅烷骨架膜层浸泡初期不能有效的阻挡Cl−进入渗入,而适当的添加大分子葛根素有助于提高SCA膜的致密性,阻挡溶液离子继续渗透,进而提高膜层的耐蚀性。

|
| 图 7 载不同浓度葛根素膜层的阻抗图 Figure 7 Impedance diagrams of coatings with puerarin under different concentrations |
| Coatings | Ecorr / V | Icorr / (μA·cm−2) | Rs / Ω | Rp0 / Ω | Qc1 / (μF·cm−2) | Rp1 / Ω | Qc2 / (μF·cm−2) |
| UMAO | −1.585±0.14 | 7.804±1.3 | 200 | 26 394 | 0.042 | ||
| SCA | −1.588±0.12 | 5.104±0.09 | 1000 | 30 000 | 0.256 | 31 000 | 0.256 |
| 1.2 mg/mL | −1.561±0.17 | 0.231±0.12 | 1000 | 186 840 | 0.058 | ||
| 2.0 mg/mL | −1.545±0.09 | 0.212±0.15 | 1000 | 214 940 | 0.069 |
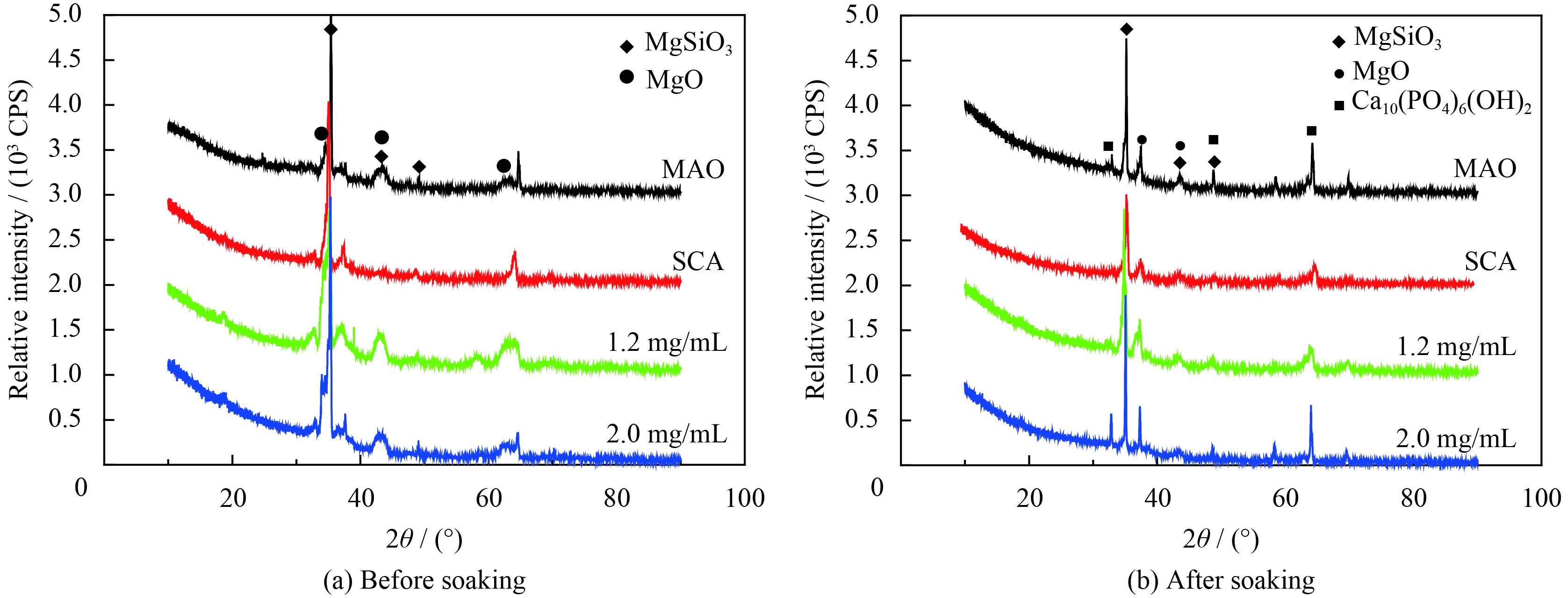
图8是载不同浓度葛根素膜层浸泡前后的XRD图谱。图9和图10是载不同浓度葛根素膜层浸泡7 d、11 d的SEM形貌。表2是膜层在SBF溶液浸泡后的Ca/P质量比。
浸泡前表面的主相为MgSiO3,MgO,在浸泡11 d后,MgSiO3,MgO的主峰强度(34.8°,42.9°)下降,表明在浸泡过程中膜层发生了降解,MgO在62.3°的峰基本消失。但UMAO和添加2 mg/mL葛根素组在32.9°,64.1°的峰增强,未进行体外模拟浸泡时膜层没有Ca元素(见图2),体外模拟7 d和11 d,膜层表面有Ca元素产生,且Ca/P增加,并且Mg元素含量相对于浸泡前都明显下降(见表2)。因此,推断经体外模拟后膜层表面有HA生成。
SEM观察UMAO浸泡7 d,11 d表面依然清晰看到微弧氧化产生的小孔,在第11天时,表面有一层白色沉积物产生,这是由于体液中Ca2+,
|
| 图 8 载不同浓度葛根素膜层在模拟体液浸泡前后的XRD图谱 Figure 8 XRD patterns of coatings with puerarin under different concentrations before and after soaking in SBF |

|
| 图 9 载不同浓度葛根素膜层浸泡7天的SEM形貌 Figure 9 SEM images of coatings with puerarin under different concentrations after soaking for 7 days |

|
| 图 10 载不同浓度葛根素膜层浸泡11天的SEM形貌 Figure 10 SEM images of coatings with puerarin under different concentrations after soaking for 11 days |
在模拟体液浸泡过程中,模拟体液最终会渗透到镁基体,引起镁的腐蚀,金属镁在模拟体液中发生析氢腐蚀,对于在硅酸盐体系下,微弧氧化表面的主相为MgSiO3,MgO,在表面又添加一层载药SCA膜层,在模拟体液中发生腐蚀的过程如下:载药SCA膜层开始对模拟体液有一定的阻挡作用,但是膜层在浸泡下也会发生降解,此时葛根素溶解到体液中,SCA膜层发生降解:
| Mass fraction
of element / % |
7 days | 11 days | |||||||
| UMAO | SCA | 1.2 mg / mL | 2.0 mg / mL | UMAO | SCA | 1.2 mg / mL | 2.0 mg / mL | ||
| Mg | 35.12 | 26.32 | 11.87 | 15.94 | 21.07 | 12.15 | 22.46 | 19.96 | |
| O | 39.13 | 42.53 | 44.25 | 39.26 | 38.23 | 35.57 | 37.73 | 39.61 | |
| Ca | 6.64 | 10.77 | 21.13 | 16.32 | 17.11 | 18.10 | 10.84 | 11.08 | |
| P | 5.50 | 9.62 | 13.97 | 12.24 | 12.76 | 12.56 | 8.88 | 8.84 | |
| Ca/P | 1.20 | 1.11 | 1.51 | 1.33 | 1.34 | 1.44 | 1.22 | 1.25 | |
Si−O−Mg+H2O→Si−OH+Mg−OH (1)
Si−O−Si+H2O→2Si−OH (2)
随着浸泡时间的延长发生:
MgSiO3+2OH−→SiO32−+Mg(OH)2 (3)
MgO+H2O→Mg(OH)2 (4)
模拟体液通过微孔渗透到镁基体,发生析氢腐蚀,使膜层周围的pH升高:
阳极:Mg→Mg2+ +2e− (5)
阴极:2H2O+2e−→H2+2OH− (6)
这就导致了由于体液的浸泡,MgSiO3,MgO的峰在浸泡11 d下降,且Cl−对Mg的腐蚀至关重要,Cl−会争夺氧离子的附着位点导致如下反应的发生:
2Cl−+Mg(OH)2→MgCl2+2OH− (7)
OH−不断富集,这样Ca,P离子在膜层周围由于电荷的吸引在表面发生矿化,最终促进羟基磷灰石的生成。
10CaHPO4+2H2O→Ca10(PO4)6(OH)2↓+4H3PO4 (8)
3 结 论(1) 纯镁UMAO膜层主相为MgO相和MgSiO3,浸渍硅烷出现Si−OH振动峰和Si−O−Si骨架吸收峰,添加葛根素有苯环的弯曲振动和苯环中−C−H−的弯曲振动峰出现,说明加入葛根素的硅烷水解液浸入膜层孔隙和表面,发生了偶联,进而对UMAO膜层实现了封孔作用。
(2) 相对于UMAO,添加葛根素的SCA膜层接触角度增加48°,自腐蚀电位提高20~40 mV,自腐蚀电流降低1个数量级。阻抗是SCA组的3~3.5倍,是UMAO组的7~8倍,复合膜层的耐蚀性显著提高。
(3) 模拟体液浸泡过程中,载药量为1.2 mg/mL时,羟基磷灰石相在7 d生成,且Ca/P比达到1.55,生物活性远高于UMAO和SCA组。
| [1] | HAGHSHENAS M. Mechanical characteristics of biodegradable magnesium matrix composites: A review[J]. Journal of Magnesium & Alloys, 2017, 5(2): 189-201 |
| [2] | ZHANG Y, FEYERABEND F, TANG S, et al. A study of degradation resistance and cytocompatibility of super-hydrophobic coating on magnesium[J]. Materials Science & Engineering C, 2017, 78: 405-412. |
| [3] | TANG H, GAO Y. Preparation and characterization of hydroxyapatite containing coating on AZ31 magnesium alloy by micro-arc oxidation[J]. Journal of Alloys & Compounds, 2016, 688: 699-708. |
| [4] | JIAN S Y, LEE J L, LEE H B, et al. Influence of electroless plating on the deterioration of the corrosion resistance of MAO coated AZ31B magnesium alloy[J]. Journal of the Taiwan Institute of Chemical Engineers, 2016, 68: 496-505. |
| 点击浏览原文 | |
| [5] |
李慕勤, 刘江, 蔡丁森, 等. 纯镁超声微弧氧化-HF-Na2SiO3复合处理对生物膜层的影响[J]. 中国表面工程, 2014, 27(3): 50-56.
LI M Q, LIU J, CAI D S, et al. Effect of pure magnesium ultrasonic micro-arc oxidation-HF-Na2SiO3 compounded treatment on the bio-coating[J]. China Surface Engineering, 2014, 27(3): 50-56 (in Chinese). |
| 点击浏览原文 | |
| [6] | GOLSHIRAZI A, KHARAZIHA M, GOLOZAR M A. Polyethylenimine/kappa carrageenan: Micro-arc oxidation coating for passivation of magnesium alloy[J]. Carbohydrate Polymers, 2017, 167: 185-195. |
| 点击浏览原文 | |
| [7] | CHEN C, DONG S, HOU R, et al. Insight into the anti-corrosion performance of electrodeposited silane/nano-CeO2, film on carbon steel[J]. Surface & Coatings Technology, 2017, 326: 183-191. |
| [8] | GU X N, GUO H M, WANG F, et al. Degradation, hemolysis, and cytotoxicity of silane coatings on biodegradable magnesium alloy[J]. Materials Letters, 2017, 193: 266-269. |
| 点击浏览原文 | |
| [9] | ZHU R L, JIN Z, WEN G. Effect of silane on galvanic corrosion between EW75 magnesium alloy and TC4 alloy[J]. Rare Metal Materials & Engineering, 2015, 44(8): 1838-1844. |
| [10] | ZHU H, YUE L, ZHUANG C, et al. Fabrication and characterization of self-assembled graphene oxide/silane coatings for corrosion resistance[J]. Surface & Coatings Technology, 2016, 304: 76-84. |
| [11] | CÓRDOBA L C, MONTEM M F, CORADIN T. Silane/TiO2, coating to control the corrosion rate of magnesium alloys in simulated body fluid[J]. Corrosion Science, 2016, 104: 152-161. |
| 点击浏览原文 | |
| [12] | CHEN C, DONG S, HOU R, et al. Insight into the anti-corrosion performance of electrodeposited silane/nano-CeO2, film on carbon steel[J]. Surface & Coatings Technology, 2017, 326: 181-191. |
| [13] | ROUZMEH S S, NADERI R, MAHDAVIAN M. Steel surface treatment with three different acid solutions and its effect on the protective properties of the subsequent silane coating[J]. Progress in Organic Coatings, 2017, 112: 133-140. |
| 点击浏览原文 | |
| [14] | MAHDAVIAN M, RAMEZANZADEH B, AKBARIAN M, et al. Enhancement of silane coating protective performance by using a polydimethylsiloxane additive[J]. Journal of Industrial & Engineering Chemistry, 2017, 55: 244-252. |
| [15] | CORDOBA L C, MONTEMOR M F, CORADIN T, et al. Silane/TiO2 coating to control the corrosion rate of magnesium alloys in simulated body fluid[J]. Corrosion Science, 2016, 104: 152-161. |
| 点击浏览原文 | |
| [16] | EJENSTAM L, SWERIN A, PAN J, et al. Corrosion protection by hydrophobic silica particle-polydimethylsiloxane composite coatings[J]. Corrosion Science, 2015, 99: 89-97. |
| 点击浏览原文 | |
| [17] | DWORSKY E M, HEGDE V, LOFTIN A H, et al. Novel in vivo mouse model of implant related spine infection[J]. Journal of Orthopaedic Research Official Publication of the Orthopaedic Research Society, 2017, 35(1): 193-199. |
| 点击浏览原文 | |
| [18] | JIA W, WU G, LIU X, et al. A decomposable silica-based antibacterial coating for percutaneous titanium implant[J]. International Journal of Nanomedicine, 2017, 12: 371-379. |
| 点击浏览原文 | |
| [19] | FERRARIS S, SPRIANO S. Antibacterial titanium surfaces for medical implants[J]. Materials Science & Engineering C Materials for Biological Applications, 2016, 61: 965-978. |
| [20] | HAQUE B M M, HAQUE M N, MOHIBBULLAH M, et al. Radix puerariae modulates glutamatergic synaptic architecture and potentiates functional synaptic plasticity in primary hippocampal neurons[J]. Journal of Ethnopharmacology, 2017, 209: 100-107. |
| 点击浏览原文 | |
| [21] | HUANG Q, ZHANG H, XUE D. Enhancement of antioxidant activity of radix Puerariae and red yeast rice by mixed fermentation with monascus purpureus[J]. Food Chemistry, 2017, 226: 89-94. |
| 点击浏览原文 | |
| [22] |
晏雨露, 徐驿, 赵继会, 等. 微针辅助条件下葛根素微乳的经皮吸收研究[J]. 中草药, 2017, 48(1): 95-101.
YAN Y L, XU Y, ZHAO J H, FENG N P, et al. Enhancement of transdermal absorption of puerarin by microneedle-assisted microemulsion[J]. Chinese Traditional and Herbal Drugs, 2017, 48(1): 95-101 (in Chinese). |
| 点击浏览原文 | |
| [23] |
吴轶, 刘文惠, 黄芳, 等. 葛根总黄酮与葛根素提取工艺优化及增强结肠炎大鼠抗氧化能力[J]. 现代食品科技, 2017, 33(10): 117-126.
WU Y, LIU W H, HUANG F, et al. Optimization of extraction technology of total flavonoids and puerarin in rdix puerariae and their enhanced antioxidant capacity in colitis rats[J]. Modern Food Science and Technology, 2017, 33(10): 117-126 (in Chinese). |
| 点击浏览原文 | |
| [24] | CHEN J, CHEN P, QI H, et al. Puerarin affects bone biomarkers in the serum of rats with intrauterine growth restriction[J]. Journal of Traditional Chinese Medicine, 2016, 36(2): 211-216. |
| 点击浏览原文 | |
| [25] | YUAN S Y, SHENG T, LIU L Q, et al. Puerarin prevents bone loss in ovariectomized mice and inhibits osteoclast formation in vitro[J]. Chinese Journal of Natural Medicines, 2016, 14(4): 265-269. |
| 点击浏览原文 | |
| [26] |
蔡云云, 李慕勤, 肖月, 等. 纯钛微弧氧化载葛根素生物膜层生物相容性研究[J]. 中国体视学与图像分析, 2017, 22 (1): 37-44.
CAI Y Y, LI M Q, XIAO Y, et al. Biocompatibility of puerarin biofilm with pure titanium micro-arc oxidation[J]. Chinese Journal of Stereology and Image Analysis, 2017, 22 (1): 37-44 (in Chinese). |
| 点击浏览原文 | |
| [27] |
李慕勤, 马臣, 张爱琴, 等. 镁、钛表面超声微弧氧化载银抗菌生物活性涂层制备方法: 200910072105.7[P]. 2011-12-07.
LI M Q, MA C, ZHANG A Q, et al. Magnesium, titanium surface ultrasound micro-arc oxidation silver antibacterial bioactive coating preparation: 200910072105.7[P]. 2011-12-07 (in Chinese). |
| [28] |
李慕勤, 彭书浩, 王晶彦, 等. 一种纯钛口腔种植体微弧氧化-多巴胺偶联载中药涂层的制备方法: 201611034630.6[P]. 2017-03-22.
LI M Q, PENG S H, WANG J Y, et al. Preparation method of traditional Chinese medicine pueraria for titanium alloy dental implant: 201611034630.6[P]. 2017-03-22 (in Chinese). |



