2. 南通河海大学海洋与近海工程研究院,江苏 南通 226019
2. Nantong Hohai University Ocean and Offshore Engineering Research Institute, Nantong 226019, Jiangsu
近年来,环境污染问题已引起全世界的广泛关注。在环境污染治理的研究过程中,研究者们发现一些半导体光催化材料可在不产生二次污染的情况下用于降解有机污染物。常见的半导体催化材料以金属氧化物或硫化物居多,如TiO2、ZnO、CdS、ZnS等[1-3]。TiO2因化学性质稳定、无毒,具有较高的光电转换效率,可有效去除大气和水中的污染物而成为解决环境污染问题的一种理想材料[4-6]。TiO2的光催化降解污染物性能与其形态密切相关。一维纳米TiO2与零维TiO2纳米颗粒相比,具有更大的比表面积、更强的吸附能力、更有利于电子传输的结构特征以及更高的光电转换效率。而在可控制备一维纳米TiO2材料的基础上进一步获得的纳米管阵列不仅拥有一维纳米TiO2的特征,并且回收利用更方便。TiO2纳米管阵列这种独特的物理、光学和电学性能,使其成为光催化降解材料的研究热点。
目前,TiO2纳米管阵列最常用的制备方法主要包括模板法[7]、水热合成法[8]、阳极氧化法[9]和溶胶-凝胶法[10]等。其中,单独采用溶胶-凝胶法制备纳米TiO2往往无法得到有效的管状结构,通常需与其他方法相结合使用。而阳极氧化法适合制备在Ti基体上负载的TiO2纳米管阵列,纳米管与Ti基底连接紧密,且具有较高的长径比和高的比表面积,较模板法和水热法体现出明显的优势[11-13]。2001年,Grimes等[13]以Ti为基底,通过阳极氧化法成功制备出高度有序的TiO2纳米管阵列后,以TiO2纳米管为代表的一维管状阵列结构的研究迅速开展起来[14-16]。电解质溶液成分、阳极氧化时间、温度、pH值等试验参数对TiO2纳米管阵列的形貌、管长和管径大小的影响,以及管形的变化对其光催化降解能力的影响成为近十几年研究的热点之一。相关研究表明,电解液的性质是决定TiO2纳米管阵列形貌的主要因素之一。有机电解液体系中含水量越少,TiO2纳米管管壁越光滑[17-18],当电解液一定时,阳极氧化电压在一定范围内增大可使TiO2纳米管管长和管径随之增大[18]。在以乙二醇或丙三醇为有机溶剂的电解液中进行阳极氧化制备TiO2纳米管阵列,易于获得较长的纳米管,在一定范围内,TiO2纳米管管长增大有利于增强TiO2纳米管阵列的光催化降解能力,TiO2纳米管阵列结构越有序,形貌越完整,吸收的光也越多。因此,适当延长TiO2纳米管管长,改善TiO2纳米管阵列结构有序性和形貌完整性,有望提升TiO2纳米管阵列的光催化降解能力。
研究者们在以乙二醇为有机溶剂的电解液体系中阳极氧化制备TiO2纳米管阵列时发现,采用一次阳极氧化法制备TiO2纳米管阵列时,材料表面存在大量劈裂的絮状物,而采用二次阳极氧化法制备TiO2纳米管阵列,阵列有序度和形貌完整度得到显著改善,在合适的二次阳极氧化工艺下可获得表面平整、相互平行排列且垂直于基底生长的有序TiO2纳米管[19]。然而,在以丙三醇为有机溶剂的电解液体系中阳极氧化制备TiO2纳米管阵列,能否采用二次阳极氧化法来改善阵列的有序性和形貌完整性并不清楚,也未见相关研究报道。TiO2纳米管阵列形貌还与后续的退火处理工艺有关,不同阳极氧化条件下制备的纳米管阵列的形貌随退火温度和退火时间的变化规律存在一定差异[20-21]。为此,文中在以丙三醇作为有机溶剂的电解液中,通过一次阳极氧化法和二次阳极氧化法在Ti基体表面制备TiO2纳米管阵列,研究阳极氧化方式、阳极氧化工艺参数(氧化电压、氧化时间)及退火温度对阵列形貌的影响。
1 试 验 1.1 TiO2纳米管阵列的制备将Ti薄板(纯度>99.6%)裁剪为15 mm×10 mm×0.1 mm的片状,分别用丙酮、无水乙醇、蒸馏水依次超声清洗10 min去除Ti片表面的油污等杂质,随后在鼓风干燥箱中进行干燥。以预处理的Ti片作为阳极,Pt电极为阴极,电极间距为2 cm,使用导线连接装置,形成闭合回路,以直流稳压电源提供直流电,采用含质量分数0.5%NH4F的丙三醇-水溶液(丙三醇/水体积比为4∶1)作为电解液,控制不同的氧化工艺参数于室温下进行阳极氧化试验。阳极氧化结束后,将阳极氧化后的Ti片放在无水乙醇中清洗掉表面的电解液,随后置于蒸馏水中超声清洗,再在鼓风干燥箱中进行干燥。
二次阳极氧化法包括两段阳极氧化过程,Ti片的预处理和电解液成分同一次阳极氧化法,从阳极电夹上取下一次阳极氧化后的Ti片,放在蒸馏水中超声至Ti片上的纳米管阵列薄膜完全剥离,暴露出银白色的Ti基底,烘干后进行第二次阳极氧化。表1和表2分别所示的是一次阳极氧化法和二次阳极氧化法制备TiO2纳米管阵列的工艺参数。将干燥后的阳极氧化试样置于箱式电阻炉中进行退火处理,升温速率为10 ℃/min,在450 ℃保温120 min后随炉冷却。为了研究退火温度对纳米管阵列形貌的影响,还以相同的方式对在优化阳极氧化工艺条件下制得的纳米管阵列进行了500 ℃、600 ℃退火处理。
1.2 TiO2纳米管阵列的表征使用Hitachi-S4800型冷场发射扫描电子显微镜对样品的形貌进行观察,利用Bruker Dimension Icon with ScanAsyst原子力显微镜对样品表面粗糙度进行测定。
| No. | Oxidation voltage / V | Oxidation time / min |
| 1 | 5 | 120 |
| 2 | 10 | 120 |
| 3 | 15 | 120 |
| 4 | 20 | 120 |
| 5 | 25 | 120 |
| No. | The first step | The second step | ||
| Oxidation
voltage / V |
Oxidation
time / min |
Oxidation
voltage / V |
Oxidation
time / min |
|
| 6 | 10 | 30 | 10 | 120 |
| 7 | 15 | 30 | 15 | 120 |
| 8 | 20 | 30 | 20 | 120 |
| 9 | 25 | 30 | 25 | 120 |
| 10 | 20 | 15 | 20 | 120 |
| 11 | 20 | 30 | 20 | 120 |
| 12 | 20 | 45 | 20 | 120 |
| 13 | 20 | 60 | 20 | 120 |
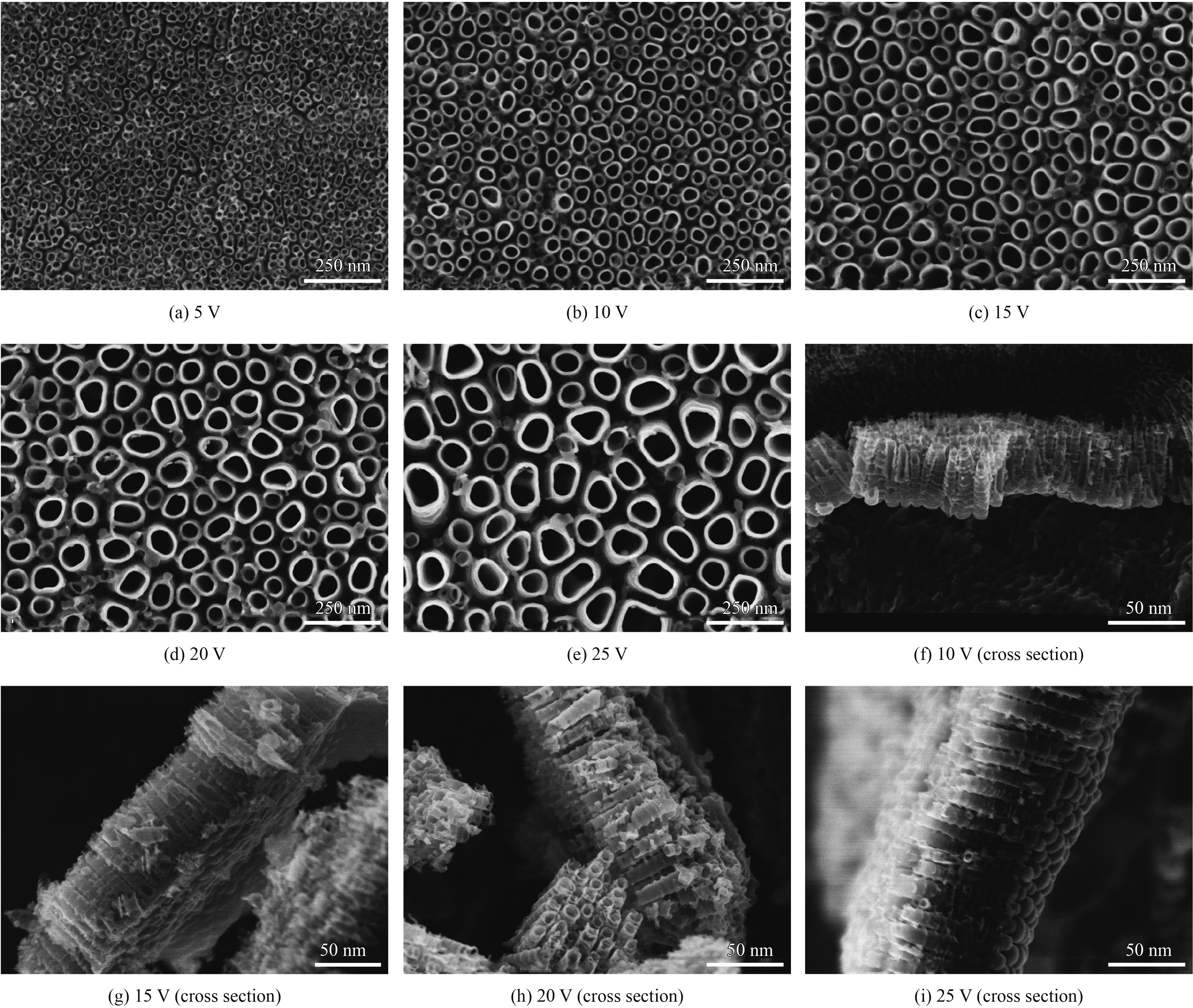
图1所示的是采用一次阳极氧化法将Ti片在不同电压下氧化120 min所制得的TiO2纳米管阵列的显微形貌,不同电压下制得的TiO2纳米管阵列其管径如表3所示。可以看出,TiO2纳米管的平均管径随电压增大而依次增大,电压从5 V升到25 V,平均管径从约25 nm增长到约80 nm。氧化电压为5 V时(见图1(a)),纳米管管径非常小,管壁之间存在明显的相互粘连,这是由于氧化电压过小,电解液对Ti片的腐蚀不够。氧化电压为10~25 V时,由图1(b)~(e)可知,除管径大小不同,TiO2纳米管阵列表面形貌基本类似,管口近似圆形或椭圆形,壁厚均匀。
通过扫描电子显微镜对所制得的TiO2纳米管阵列侧面观察以及原子力显微镜对阵列表面粗糙度的测定发现,阵列表面均有一定的不平整度。5、10、15、20和25 V下制得的TiO2纳米管阵列表面的粗糙度分别约为96.0、87.9、50.7、23.1和87.6 nm。相比而言,20 V/120 min条件下阳极氧化制得的纳米管阵列表面平整度较好。
此外,在不同阳极氧化电压下制得的TiO2纳米管还具有“竹节状”结构特征。图1(f)~(i)分别给出了在10~25 V阳极氧化制得的TiO2纳米管侧面形貌,由图可清晰地看到竹节状纳米管的具体形态。这种结构产生的原因可能是丙三醇的加入使电解液粘度增大,溶液中离子的扩散速度变慢,纳米管微孔中的溶液出现浓度差而引起F−扩散不均匀,溶解速度不一致,因而长成的纳米管管壁部分被溶解。这种结构可增加单个纳米管的比表面积,有望提高TiO2纳米管阵列的光催化降解能力。由侧面形貌还可看出纳米管管长随氧化电压而改变。
以上现象表明TiO2纳米管阵列的表面平整度和管长可通过改变氧化电压进行调控,其匹配恰当将有利于阵列光催化性能的提升。
在不同氧化电压制备的TiO2纳米管平均管径变化如图2所示,可以看出氧化电压与纳米管平均管径间存在良好的线性关系。Macak等人[22]在阳极氧化法制备TiO2纳米管时也出现类似的规律。纳米管平均管径随电压增大而增大,可能是电压升高加快了电解质溶液中F−向氧化膜表面转移的速度,增强了阳极氧化速度引起的。
|
| 图 1 一次阳极氧化法在不同氧化电压条件下制备的TiO2纳米管阵列显微形貌 Figure 1 Micro-morphologies of TiO2 nanotube arrays prepared at different oxidation voltage by one-step anodic oxidation |
| No. | Voltage / V | Tube diameter / nm |
| 1 | 5 | 25−30 |
| 2 | 10 | 25−50 |
| 3 | 15 | 45−70 |
| 4 | 20 | 50−80 |
| 5 | 25 | 60−100 |
由于阳极氧化使用的Ti片表面有一定的粗糙度,而且在氧化过程中缺陷部位导致Ti片上各处的电场密度不同,致使氧化速率不同,纳米管的生长速率不一致,最终得到的一次阳极氧化TiO2纳米管阵列表面呈现如图3中part B区所示的不平整现象。但在蒸馏水中超声清洗去除一次阳极氧化得到的纳米管后留下的基底可以呈现相对较为平整的印迹表面(如图3中part A区),试以此作为模板进行第二次阳极氧化,以期获得表面平整、排列规则均匀的TiO2纳米管阵列。

|
| 图 2 一次阳极氧化制备的TiO2纳米管阵列平均管径与氧化电压的关系 Figure 2 Relationship between the average tube diameter of the TiO2 nanotube arrays and the oxidation voltage by one-step anodic oxidation |

|
| 图 3 一次阳极氧化法制得的TiO2纳米管阵列超声去除部分纳米管后的表面形貌(Part A: 超声去除纳米管阵列后的基底形貌; Part B: 原纳米管阵列表面形貌) Figure 3 Surface morphology of TiO2 nanotube array prepared by one-step anodic oxidation after removing part of the nanotubes by ultrasonic (Part A: the substrate morphology after removing the nanotubes by ultrasonic; Part B: the original surface morphology of the nanotubes array) |
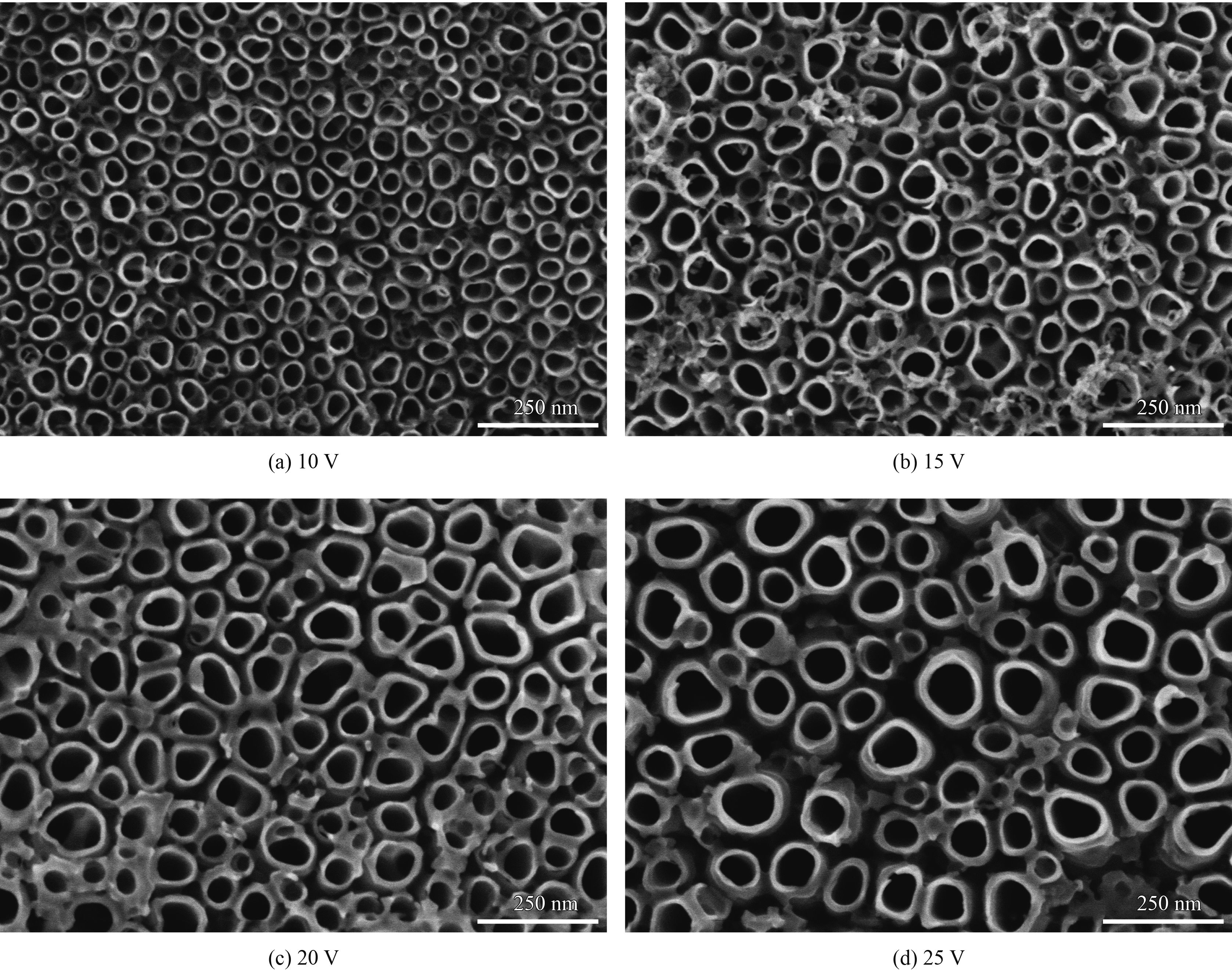
图4所示的分别是在10、15、20和25 V下采用二次阳极氧化法(第一次阳极氧化时间为30 min,第二次阳极氧化时间为120 min)制得的TiO2纳米管阵列的微观形貌。对比图1和图4可知,在相同的氧化电压下,采用一次阳极氧化法和二次阳极氧化法制得的TiO2纳米管阵列平均管径大小基本相同,二次阳极氧化法并没有得到表面更加规整、管径更为均匀、管形更为完整的纳米管阵列。
2.2.2 二次阳极氧化法中第一次阳极氧化时间对纳米管阵列形貌的影响图5所示的是阳极氧化电压为20 V,第一次阳极氧化时间分别为15、30、45和60 min,第二次氧化时间为120 min的二次阳极氧化法制得的TiO2纳米管阵列表面形貌。可以发现,随着第一次氧化时间的增加,纳米管管口圆整度有所提升,管壁变薄,管口清晰,管口和管间的絮状物有所减少,这部分絮状物可能是由于少数纳米管因过度腐蚀遭到破坏而形成的。对4组纳米管阵列表面粗糙度测试发现,随第一次氧化时间延长,其粗糙度依次为166 nm、82.5nm、69.6 nm和62.4 nm,即纳米管阵列表面越平整。但与同一电压的一次阳极氧化法所制备的纳米管阵列相比,可知,二次阳极氧化法制得的TiO2纳米管阵列的有序程度和表面平整度并没有得到有效改善。
二次阳极氧化法制备TiO2纳米管阵列不能有效改善其有序度和表面平整度可能有以下几方面原因。
(1)氧化时间的影响。若第一次阳极氧化时间过短,尚未腐蚀出大小、形状均匀排列整齐的孔洞,在此基础上进行第二次阳极氧化得到的纳米管其形貌将受到很大影响。第一次氧化时间和第二次氧化时间的合理组合对纳米管形貌的影响有待进一步研究。
(2)电解液种类的影响。在以乙二醇作为有机溶剂的电解液中通过二次阳极氧化法可以制备出较一次阳极氧化更为均匀有序的TiO2纳米管和孔洞,纳米管外壁平滑[23-24]。而当电解液以丙三醇作为有机溶剂时,阳极氧化获得的纳米管呈“竹节状”结构特征,管形的这种改变也可能会影响到最终的管口形貌。可见,TiO2纳米管形貌的改性效果受电解液性质(粘度、介电常数)影响。
(3)电解液浓度的影响。在阳极氧化过程中,会消耗电解液中的F−、H+等,使电解液中离子的浓度分布不同,随着时间的延长,Ti片处后续的离子可能供给不足,使得Ti基体上腐蚀不均匀,从而影响纳米管阵列的均匀性和有序性。
(4)第一次阳极氧化孔和第二次氧化孔不重合。在二次阳极氧化中第一次氧化时Ti片所夹的位置和第二次所夹位置若有偏差,则第一次氧化反应过程中的电场分布与第二次的电场分布方向不能完全重合,于是两次氧化所得到的孔洞也不重合。所以要保证两次氧化所腐蚀的位置尽量相同。
|
| 图 4 二次阳极氧化法在不同氧化电压条件下制备的TiO2纳米管阵列显微形貌 Figure 4 Micro-morphologies of TiO2 nanotube arrays prepared at different oxidation voltage by two-step anodic oxidation |

|
| 图 5 20 V电压下不同第一次阳极氧化时间的二次阳极氧化法得到的TiO2纳米管阵列显微形貌 Figure 5 Micro-morphologies of TiO2 nanotube arrays prepared at 20V for different first oxidation time by two-step anodic oxidation |
由以上分析可知,采用一次阳极氧化方法在20 V/120 min条件下制得的TiO2纳米管阵列形貌较优。为考查退火温度对形貌的影响,分别在450、500和600 ℃对其进行退火处理2 h,图6给出了不同温度退火处理后纳米管阵列的显微形貌。450 ℃和500 ℃退火后,纳米管阵列形貌变化不明显,当退火温度升至600 ℃,纳米管层/钛金属基体界面处有较为致密的热氧化物层形成,其厚度约250~300 nm左右,纳米管长度较前两者变短。Anca Mazare等人认为该热氧化物层是金红石层[20]。根据前期的研究[25],未退火时,纳米管阵列为无定形,450 ℃和500 ℃退火处理,纳米管阵列主要为锐钛矿相,600 ℃退火处理,则为金红石和锐钛矿混合相,纳米管阵列形貌随退火温度的变化应与晶型变化和原子扩散有关。

|
| 图 6 20 V/120 min下制得的TiO2纳米管阵列经不同温度退火后的显微形貌 Figure 6 Micro-morphologies of TiO2 nanotube array prepared at 20 V/120 min after annealing at different temperature |
(1) 以NH4F-丙三醇-水溶液为电解液,采用一次阳极氧化法可制得有序的TiO2纳米管阵列,TiO2纳米管呈竹节状结构特征,纳米管的平均管径和管间距随阳极氧化电压升高而增大,在20 V/120 min氧化条件下制得的TiO2纳米管阵列相对较优,其表面平整度高。
(2) 以NH4F-丙三醇-水溶液为电解液,在相同氧化电压下采用二次阳极氧化法制得的TiO2纳米管阵列与一次阳极氧化法制得的TiO2纳米管阵列相比,阵列的有序程度和表面平整度并未得到有效改善。这可能是源于氧化时间、电解液种类和浓度,以及第一次阳极氧化孔和第二次阳极氧化孔不完全重合等对纳米管生长造成的影响。
(3) 退火温度低于500 ℃,温度变化对TiO2纳米管阵列的形貌影响不明显,600 ℃退火会促进纳米管层/钛金属基体界面处的热氧化物层生长。
| [1] | YANG X D, WANG Y Q, WANG Z S, et al. Preparation of CdS/TiO2 nanotube arrays and the enhanced photocatalytic property[J]. Ceramics International, 2016, 42: 7192-7202. |
| 点击浏览原文 | |
| [2] | LI Y C, MA Q, HAN J, et al. Controllable preparation, growth mechanism and the properties research of TiO2 nanotube arrays[J]. Applied Surface Science, 2014, 297: 103-108. |
| 点击浏览原文 | |
| [3] | MA Q, WANG Y Q, KONG J H, et al. Tunable synthesis, characterization and photocatalytic properties of various ZnS nanostructures[J]. Ceramics International, 2016, 42(2): 2854-2860. |
| 点击浏览原文 | |
| [4] |
房治, 周庆祥. TiO2纳米管阵列在环境领域的研究进展[J]. 化学学报, 2012, 17(17): 1767-1774.
FANG Z, ZHOU Q X. Research advances of TiO2 nanotube array in environmental field[J]. Acta Chimica Sinica, 2012, 17(17): 1767-1774 (in Chinese). |
| 点击浏览原文 | |
| [5] | LIU H J, LIU G G, FAN J, et al. Photoelectro catalytic degradation of 4,4′-dibromobiphenyl in aqueous solution on TiO2 and doped TiO2 nanotube arrays[J]. Chemosphere, 2011, 82: 43-47. |
| 点击浏览原文 | |
| [6] |
王后锦, 吴晓婧, 王亚玲, 等. 二氧化钛纳米管阵列光电催化同时降解苯酚和Cr(VI)[J]. 催化学报, 2011, 32(4): 637-642.
WANG H J, WU X J, WANG Y L, et al. Simultaneous removal of phenol and Cr(VI) by TiO2 nanotube array photoelectrocatalysis[J]. Chinese Journal of Catalysis, 2011, 32(4): 637-642 (in Chinese). |
| [7] | KANG T S, SMITH A P, TAYLOR B E, et al. Fabrication of highly-ordered TiO2 nanotube arrays and their use in dye-sensitized solar cells[J]. Nano Letters, 2009, 9(2): 601-606. |
| 点击浏览原文 | |
| [8] | KASUGA T, HIRAMATSU M, HOSON A, et al. Formation of titanium oxide nanotube[J]. Langmuir, 1998, 14(12): 3160-3163. |
| 点击浏览原文 | |
| [9] | BALAKRISHNAN M, NARAYANAN R. Synthesis of anodic titania nanotubes in Na2SO4/NaF electrolyte: a comparison between anodization time and specimens with biomaterial based approaches[J]. Thin Solid Films, 2013, 540(4): 23-30. |
| 点击浏览原文 | |
| [10] |
李晓红, 张校刚, 力虎林. TiO2纳米管的模板法制备及表征[J]. 高等学校化学学报, 2001, 22(1): 130-132.
LI X H, ZHANG X G, LI H L. Template synthesis and characterization of TiO2 nanotubules[J]. Chemical Journal of Chinese Universities, 2001, 22(1): 130-132 (in Chinese). |
| 点击浏览原文 | |
| [11] | JAROENWORALUCK A, REGONINI D, BOWEN C R, et al. Macro, micro and nanostructure of TiO2, anodised films prepared in a fluorine-containing electrolyte[J]. Journal of Materials Science, 2007, 42(16): 6729-6734. |
| 点击浏览原文 | |
| [12] | MACAK J M, TSUCHIYA H, GHICOV A, et al. TiO2 Nanotubes: self-organized electrochemical formation, properties and applications[J]. Current Opinion in Solid State & Materials Science, 2007, 11(1): 3-18. |
| [13] | GONG D, GRIMES C A, VARGHESE O K, et al. Titanium oxide nanotube arrays prepared by anodic oxidation[J]. Journal of Materials Research, 2011, 16(12): 3331-3334. |
| 点击浏览原文 | |
| [14] | YAN J, ZHOU F. TiO2 nanotubes: structure optimization for solar cells[J]. Journal of Materials Chemistry, 2011, 21(26): 9406-9418. |
| 点击浏览原文 | |
| [15] | MOR G K, VARGHESE O K, PAULOSE M, et al. A review on highly ordered, vertically oriented TiO2, nanotube arrays: Fabrication, material properties, and solar energy applications[J]. Solar Energy Materials & Solar Cells, 2006, 90(14): 2011-2075. |
| 点击浏览原文 | |
| [16] | VU T H T, NGUYEN T T T, NGUYEN P H T, et al. Fabrication of photocatalytic composite of multi-walled carbon nanotubes/TiO2, and its application for desulfurization of diesel[J]. Materials Research Bulletin, 2012, 47(2): 308-314. |
| 点击浏览原文 | |
| [17] |
刘榕芳, 李萍, 王章, 等. 甘油/DMF混合体系中TiO2纳米管阵列的制备及表征[J]. 材料导报, 2014, 28(8): 13-18.
LIU R F, LI P, WANG Z, et al. Preparation and characterization of TiO2 nanotube arrays in glycerin/DMF mixed electrolyte[J]. Materials Review, 2014, 28(8): 13-18 (in Chinese). |
| 点击浏览原文 | |
| [18] | HILARIO F, ROCHE V, NOGUEIRA R P, et al. Influence of morphology and crystalline structure of TiO2 nanotubes on their electrochemical properties and apatite-forming ability[J]. Electrochimica Acta, 2017, 245: 337-349. |
| 点击浏览原文 | |
| [19] | WANG D, YU B, WANG C, et al. A novel protocol toward perfect alignment of anodized TiO2 nanotubes[J]. Advanced Materials, 2009, 21(19): 1964-1967. |
| 点击浏览原文 | |
| [20] | MAZARE A, TOTEA G, BURNEI C, et al. Corrosion, antibacterial activity and haemocompatibility of TiO2 nanotubes as a function of their annealing temperature[J]. Corrosion Science, 2016, 103: 215-222. |
| 点击浏览原文 | |
| [21] | DAS S, ZAZPE R, PRIKRYL J, et al. Influence of annealing temperatures on the properties of low aspect-ratio TiO2 nanotube layers[J]. Electrochimica Acta, 2016, 213: 452-459. |
| 点击浏览原文 | |
| [22] | MACAK J M, HILDEBRAND H, MARTEN-JAHNS U, et al. Mechanistic aspects and growth of large diameter self-organized TiO2, nanotubes[J]. Journal of Electroanalytical Chemistry, 2008, 621(2): 254-266. |
| 点击浏览原文 | |
| [23] |
余青青, 储成林, 林萍华, 等. 二氧化钛纳米管阵列的二次阳极氧化制备[J]. 稀有金属材料与工程, 2011, 40(S2): 201-205.
YU Q Q, CHU C L, LIN P H, et al. Fabrication of TiO2 nanotube arrays by a two-step anodic oxidation[J]. Rare Metal Materials and Engineering, 2011, 40(S2): 201-205 (in Chinese). |
| [24] |
肖同欣, 吴红军, 高杨, 等. 二次阳极氧化制备TiO2纳米管阵列及光催化性能研究[J]. 化学工程师, 2014, 28(5): 8-10.
XIAO T X, WU H J, GAO Y, et al. Preparation of TiO2 nanotube arrays by a two-step anodic oxidation and investigation of its photocatalytic activity[J]. Chemical Engineer, 2014, 28(5): 8-10 (in Chinese). |
| [25] |
柳堤. TiO2纳米管/棒阵列的制备、改性与光催化性能研究[D]. 南京: 河海大学, 2017: 40-41.
LIU D. Researches on preparation, modification and photocatalytic properties of TiO2 nanotube/nanrod arrays[D]. Nanjing: Journal of Hohai University, 2017: 40-41 (in Chinese). |



